서 론
옥수수(Zea mays L.)는 벼, 밀과 함께 세계 3대 식량작물로서 세계 총 곡물 생산량의 약 85%를 차지하며 매년 약 2억 톤의 단백질 공급원이 된다(Prasanna et al., 2001; Shewry, 2007). 옥수수는 전 세계인들이 곡물로부터 얻을 수 있는 총 칼로리의 약 20% 및 총 단백질의 약 15%를 제공하고 있으며 가축의 영양에도 매우 중요한 영양원이 되고 있다(Sofi et al., 2009). 옥수수 종실 단백질의 함량은 7~9%이며 이 중 zein이 총 단백질의 60~70%를 차지하고 있다(Sofi et al., 2009). Zein 단백질을 구성하고 있는 주요 아미노산은 glutamic acid 21~26%, leucine 20%, proline 10% 및 alanine 10%로 풍부하지만 필수 아미노산인 lysine과 tryptophan의 함량이 적어 사람 및 단위동물(monogastric animal)에게 영양적으로 제한 요인이 된다(Leite et al., 1999; Huang et al.,2004; Freitas et al., 2005). 이러한 영양학적 제한요인은 아이들의 초기 성장 부진, 과민성 피부 병변, 부종 및 지방간을 특징으로 하는 단백질 결핍증인 Kwashiorkor 병을 유발할 수 있다고 한다(Vivek et al., 2008). 따라서 사람뿐만 아니라 단위동물의 균형적인 영양 섭취를 위해서는 lysine과 tryptophan 함량을 증진시킬 필요가 있다(Prasanna et al., 2001). CIMMYT (국제옥수수밀연구소)는 일반옥수수와 같이 경질 배유이면서도 lysine과 tryptophan 함량을 2배 정도 높인 옥수수를 지속적으로 개발하여 왔는데, 대표적인 것이 quality protein maize (QPM)이다(Babu & Pasanna, 2013). QPM의 개발은 옥수수를 주식으로 이용하고 있는 세계 여러 나라의 빈곤층에 영양학적으로 균형 있는 식량을 제공할 수 있는 계기가 되었다. QPM으로 이유식을 만들어 영아들에게 제공한 결과 발육이 촉진되고 체중이 증가되는 효과를 얻었다고 보고된 바 있다(Graham et al., 1990; Gunaratna et al., 2010). 우리나라는 매년 약 1,000만 톤의 옥수수를 수입하고 있으며 이들은 모두 non-QPM 옥수수로서 약 80%는 사료용으로, 약 20%는 식가공용인 옥분과 전분용 등에 사용되고 있다(MAFRA, 2018). 최근 유전자변형농산물(GMO)에 대한 불신과 식품 안전성 문제로 안전 먹거리에 대한 관심이 높아지면서 국산 곡실용 옥수수에 대한 수요가 증가 하고 있으나 곡실용 옥수수 품종 및 재배 생산 기반이 미흡한 실정이다. 이와 같은 이유는 곡실용 옥수수는 수입산에 비해 가격경쟁력이 낮고 QPM옥수수와 같은 고품질 곡실용 옥수수 품종이 없었기 때문인 것으로 판단된다. 국내에서도 고품질 곡실용 옥수수를 개발하기 위한 QPM 연구가 수행되고 있으나(Choi et al., 1977; Kim et al., 2006) 아직까지 QPM 품종이 개발되지 못하고 있는 실정이다. 따라서 본 연구는 QPM 계통의 국내 적응성 검토 및 국내 기본식물과 교배를 통해 얻어진 교잡계들의 생육특성과 아미노산 함량의 변화를 검토하여 국내에 적응성이 높은 QPM 신품종을 육성하기 위한 기초자료로 활용하고자 수행하였다.
재료 및 방법
시험 재료
본 연구는 2018~2019년 수원시 권선구 소재 농촌진흥청 국립식량과학원 중부작물부 시험연구포장(수원, N126°58′ E37°15′)에서 실시하였다. 옥수수 시험 재료는 국내육성 non-QPM 계통인 KS140과 QPM 계통인 CML153 등 11계통, KS140과 CML 계통과 교배로 얻어진 11 교잡계였다(Table 1). 국내육성 non-QPM 계통인 KS140을 시험재료로 선정한 이유는 보유하고 있는 옥수수 유전자원 중 KS140이 CML 계통과 출사기가 가장 일치하였기 때문이다.
Table 1.
Major growth and seed characteristics of quality protein maize and the crossed lines.
시비량 및 재식거리
옥수수의 시비량(N-P2O5-K2O-퇴비)은 14.5-3-6-1,500 kg/10a로 시용하였으며, 질소(N)는 기비와 7~8엽기의 추비로 50:50으로 나누어 주었고, 인산(P2O5), 칼리(K2O) 및 퇴비는 전량을 기비로 시용하였다. 재식거리는 60 × 25 cm (6,600/10a)이었으며 무피복 재배를 하였고, 기타 재배관리 및 조사항목은 농촌진흥청 농업과학기술 연구조사 분석기준(RDA, 2012)을 따랐다.
일반성분
QPM 계통을 4월 18일 파종하여 8월 말 수확 후 자연 건조하여 시험용 분쇄기로 분쇄 후 분석시료로 사용하였다. 각 계통당 3 반복하여 시료를 준비하였다. 단백질 함량은 TruMac N Analyzers (Leco, Michigan, USA)로 분석하였다. 지방산 조성의 분석은 시료에 methanol : heptane : benzene : 2,2-dimethoxypropane : H2SO4 (37 : 36 : 20 : 5 : 2, v/v)을 2 mℓ 가하고 80°C로 20분 가열 후 상등액을 취해 gas chromatography (GC-2010 plus, Shimadzu, Japan)와 HP- Innowax capillary column (30 m × 0.25 mm × 0.25 μm, Agilent J&W, Wilmington, DE, USA)로 분석하였다. 지방산 표준물질은 Supelco (Bellefonte, PA, USA) FAME mix (C14-C22) 제품을 사용하였다. Starch 함량은 시료 100 mg을 칭량하여 total starch assay kit (Megazyme, Wicklow, Ireland)로 전처리하고, UV/Vis spectrometer (U-3900, Hitach, Japan)로 510 nm에서 측정하여 정량하였다. Amylose와 amylopectin 함량은 시료 25 mg을 칭량하여 amylose/amylopectin kit (Megazyme, Wicklow, Ireland)을 이용하여 전처리하고, UV/Vis spectrometer (U-3900, Hitach, Japan)로 510 nm에서 측정하여 정량하였다.
아미노산 함량
아미노산의 함량을 분석하기 위하여 시료 0.2 g에 10 ml의 6N HCl을 가하고 N2 gas로 치환시킨 후 110°C에서 24시간 HCl로 가수분해 후 No.2 여지로 여과하여 100 ml volume flask에 옮겨 넣고 Milli-Q water로 정용하였다. 이들 중 분자량이 큰 화합물을 제거시키기 위하여 0.1% TFA (solution I), methanol (80:20, solution II), methanol (70:30, solution III)으로 Sep-pak C18을 활성화시킨 후 시료용액을 통과시킨 후 EZfaast amino acid analysis kit (Phenomenex, Torrance, CA, USA)를 이용하여 전처리 한 시료는 Shimadzu GC-2010 plus를 이용하여 정량 분석하였다. 분석조건은 spit mode로 2 μl 주입하였고, injector의 온도를 250°C, FID detector는 320°C로 각각 설정하고, oven 온도를 110°C에서 320°C까지 분당 32°C로 상승시키면서 아미노산 함량을 분석하였다.
통계분석
주성분 분석은 웹기반 대사체 분석 프로그램인 MetaboAnalyst를 이용하여 수행하였다(https://www.metaboanalyst. ca; Pang et al., 2020). 각각 아미노산의 함량은 auto scaling 방식으로 변환하여 각각 아미노산 함량이 주성분 분석에 비슷한 효과를 내도록 하였다. 통계분석은 SAS 9.2 (Statistical analysis systems Inc., Raleigh, NC, USA)을 이용하여 분산분석(ANOVA)을 하였으며 던컨의 다중범위 검정(Duncan’s multiple range test)으로 5% 유의수준에서 검정하였다.
결과 및 고찰
생육특성
Table 1은 KS140, CML 계통 및 KS140과 CML 교잡계의 주요 생육 특성을 나타낸 것이다. CML 계통의 출사일수 범위는 78~90일 이었으며 CML181이 78일로 가장 빨랐고, CML157과 CML164가 90일로 가장 늦었다. CML 교잡계의 평균 출사일수는 85일 이었으며 출사일수 범위는 81~87일이었다. KS140의 출사일수와 CML 계통의 평균 출사일수, CML 교잡계의 평균 출사일수는 모두 85일로 같았으나 범위는 차이가 있는 것으로 나타났는데, 이와 같은 원인은 CML 계통 중 출사일수가 빠른 계통이 KS140과 교잡되면서 출사일수가 늦어졌고, 출사 일수가 늦은 계통은 오히려 빨라졌기 때문인 것으로 판단된다. Vasal (2002)은 라틴아메리카 41개 지역에서 CML141×CML144 등을 재배해본 결과 CML 8교잡계의 출사일수는 55~56일이라고 보고한바 있는데, 이와 같이 국내 CML 계통 및 교잡계와 약 30일 정도 출사일수가 차이를 보인 원인은 적산온도와 위도의 차이에 기인한 것으로 판단되었다. CML 계통의 출웅일수와 출사일수는 평균적으로는 3일 정도 차이가 있었으나 CML188은 6일, CML155는 7일, CML529는 8일의 차이를 보였다. 국내 계통의 출웅일수와 출사일수는 약 1~4일 범위의 차이를 보였는데, 일반적으로 개화기가 5일 이상의 차이가 있으면 selfing이 어려워서 종자 생산에 다소간 문제가 발생될 것으로 판단된다. CML계통 중 CML191의 간장과 착수고는 각각 155 cm 및 72 cm로 가장 낮았으며, CML529의 간장이 242 cm, CML164의 착수고가 139 cm로 가장 높은 것으로 나타났다. KS140과 CML계통 교잡계 중 간장은 KS140/CML529가 245 cm로 가장 높았으며, KS140/CML170이 219 cm로 가장 낮았다. 착수고는 KS140/CML164가 148 cm로 가장 높았고, KS140/CML155가 117 cm로 가장 낮았다. CML164의 착수고는 계통과 교잡계 모두에서 가장 높은 것으로 조사되었다. 과피색은 KS140이 노란색, CML 계통은 흰색과 노란색이었으며 교잡계는 CML 계통이 흰색인 경우에는 노랑과 흰색의 중간색을 나타냈다. CML 계통의 100립중은 11.9~23.0 g 범위로 CML188이 11.9 g으로 가장 가벼웠고, CML157이 23.0 g으로 가장 무거웠다. CML 교잡계는 KS140/CML188이 16.1 g으로 가장 가벼웠고, KS140/CML180이 26.2 g으로 가장 무거웠다. 백립중은 배유의 양분 저장과 관련이 있는데, CML188 계통과 교잡계는 모두 20 g이하로 저장 양분이 충분하지않아 발아에 문제가 생길 수 있다.
일반성분
Table 2는 KS140, CML 계통과 교잡계의 단백질, 지방산, 녹말, 아밀로팩틴, 아밀로스 함량을 나타낸 것이다. CML 계통의 단백질 함량은 9.1~12.0% 범위를 보였는데, 이들중 CML153의 함량이 가장 적었고, CML191의 함량이 가장 많은 것으로 나타났다. CML 교잡계의 단백질 함량은 9.1~11.1% 범위로서 KS140/CML170이 가장 적었고, KS140/CML191이 가장 많았다. 지방산 조성비율은 KS140, CML 계통과 교잡계 모두 C18:2 (linoleic acid)가 가장 많았고 C18:1 (oleic acid), C16:0 (palmitic acid), C18:0 (stearic acid), C18:3 (linolenic acid) 순 이였다. Kim et al. (2006)에 따르면 옥수수의 지방산 조성비율은 linoleic acid와 oleic acid가 주종을 이루고 palmitic acid, stearic acid 또는 linolenic acid의 순이라고 하였다. KS140의 포화지방산 비율은 18.5%였고, 불포화지방산 비율은 81.5%였다. CML 계통의 평균 포화지방산 비율은 21.4%였으며 불포화지방산 비율은 78.6%로 KS140보다 포화지방산 비율이 다소 높았다. 그러나 CML 181은 포화지방산 비율이 16.9%, 불포화지방산 비율이 83.1%로 non-QPM 계통인 KS140보다 포화지방산 비율이 낮았다. CML 교잡계의 평균 포화지방산 비율은 19.8%, 불포화지방산 함량은 80.2%로 포화지방산 함량이 KS140보다는 높았지만 CML 계통 보다는 낮았다. Kim et al. (2006)은 QPM 계통은 non-QPM 계통에 비하여 포화지방산의 비율이 19.1%로 다소 높고 불포화지방산 비율은 80.9%로 non- QPM 옥수수의 81.6%에 비하여 조성비가 낮다고 하여 본 연구의 결과는 이들의 보고와 일치하는 것으로 나타났다. CML 계통의 전분 함량은 61.1~65.8% 범위로 CML191이 가장 낮았고, CML180이 가장 높았으나 KS140의 68.5% 보다는 다소 낮음을 알 수 있었다. CML 교잡계의 전분 함량은 66.1~69.0%로 CML 계통의 범위보다는 다소 높아짐을 알 수 있었다. CML 계통의 아밀로팩틴 함량은 16.5~27.0%의 범위를 보였는데, CML529 16.5%로 가장 낮았고, CML 170이 27.0%로 가장 높은 것으로 나타났다. CML 교잡계의 아밀로팩틴 함량 범위는 18.7~20.7%였으며 KS140/CML529를 제외한 모든 교잡계에서 그 함량이 감소되는 것으로 나타났다.
Table 2.
Variation in the chemical compositions of quality protein maize and the crossed lines (Unit: %)
아미노산 조성
Table 3은 KS140, CML 계통 및 교잡계의 아미노산 조성을 비교한 것이다. KS140의 아미노산 조성은 glutamic acid이 13.03%로 가장 많았고 leucine은 9.65%이며 aspartic acid, valine, proline, alanine, serine, phenylalanine, isoleucine, glycine, threonine, lysine, histidine, tyrosine, methionine 순이었다. QPM 계통의 평균 아미노산 함량은 glutamic acid이 13.57%로 가장 많았고 aspartic acid, valine, proline, leucine, alanine, serine, lysine, phenylalanine, glycine, threonine, histidine, isoleucine, tyrosine, methionine 순이었다, QPM 교잡계의 평균 아미노산 함량은 glutamic acid이 14.48%로 가장 많았고, leucine, aspartic acid, proline, alanine, valine, phenylalanine, serine, glycine, isoleucine, lysine, threonine, histidine, tyrosine, methionine 순이었다. Glutamic acid이 KS140, CML 계통 및 교잡계에서 가장 많았지만 그 외의 아미노산은 조성비에서 조금씩 차이가 있었다. Son et al. (2012)는 국내 육성 옥수수 자식계통, F1, F2 종실의 아미노산 조성을 비교한 결과 자식 계통과 F1, F2에서 모두 glutamic acid이 각각 15.65%, 15.6%로 가장 높았으나 다른 아미노산의 조성비는 조금씩 다르다고 하였다. Kim et al. (2006)은 QPM 계통의 lysine 조성비가 1.02%로 non-QPM 계통 0.74%에 비하여 함량이 높았으며 non-QPM 계통 대비 약 38% 정도가 증가되었다고 하였다. Vivek et al. (2008)은 유전적 배경에 따라서 다를 수 있지만 배유 단백질에서 일반옥수수의 lysine 함량은 1.6~2.6% (평균 2.0%), QPM은 2.7~4.5% (평균 4.0%)로 보고하였다. Shewry (2007)은 QPM의 lysine 함량은 4.1%로 2.7%인 non-QPM보다 69% 높다고 하였다. 본 연구에서의 lysine 함량은 non-QPM인 KS140이 2.51%, QPM인 CML 계통 평균이 4.83%였으며 CML155가 6.92% 가장 높았다. 이와같은 결과는 Kim et al. (2006)의 QPM옥수수 분석에 따른 lysine 함량보다 상당히 높았으며 Vivek et al. (2008)과 Shewry (2007)이 보고한 lysine 함량보다도 약간 높았다. 이러한 결과의 차이는 유전자원 자체의 차이에 기인한다기 보다는 환경적인 원인에 기인한 것으로 판단된다. CML 교잡계 평균은 3.46%였으며 KS140/ CML164와 KS140/CML170의 lysine 함량은 각각 4.18%과 4.99%로 교배하기 전의 QPM계통인 CML164, CML170보다 높았다. 이는 모본/부본의 증식이 가능하다면 국내 계통과 QPM 계통의 직접적인 교배를 통해서도 FAO의 lysine 함량 기준인 4%를 충족할 수 있음을 보여주었다.
Table 3.
Amino acid compositions of quality protein maize and the crossed lines.
아미노산 조성 및 주성분 분석
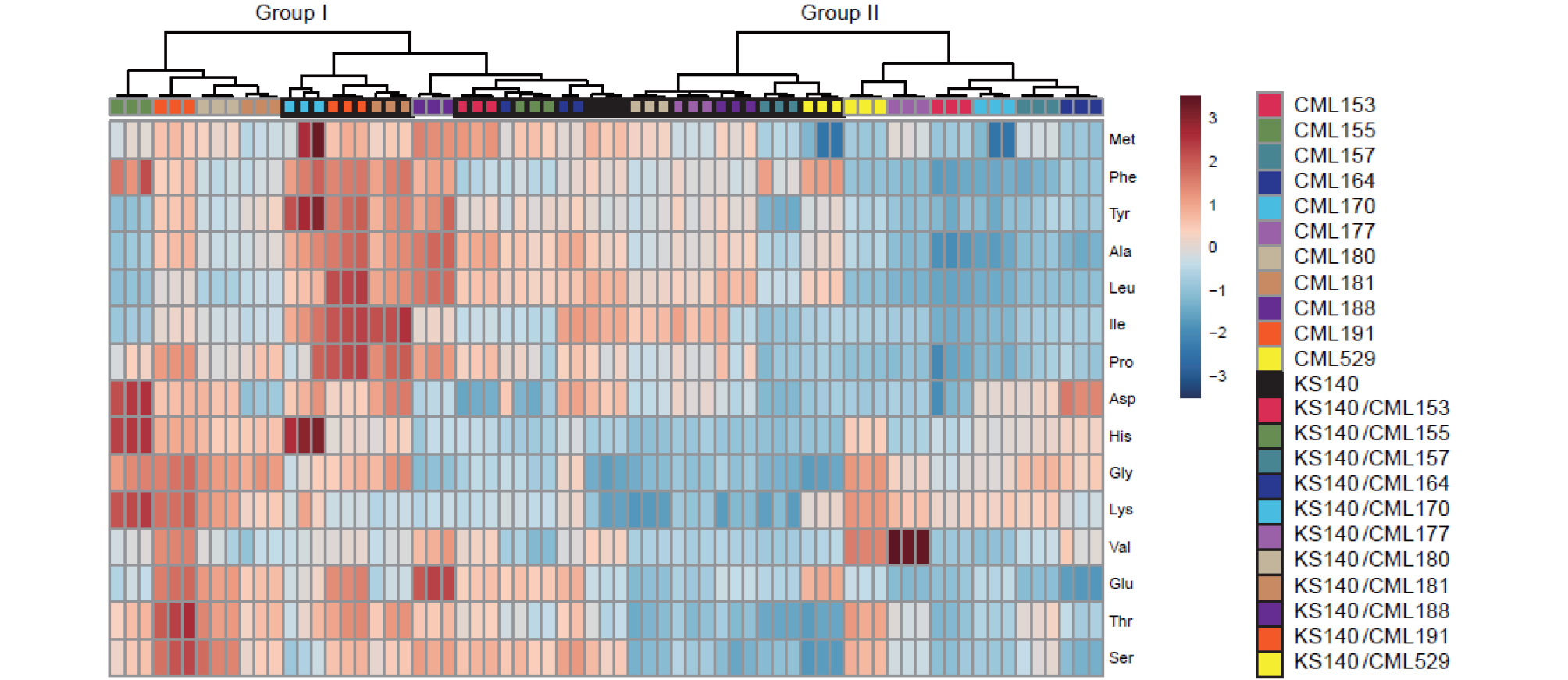
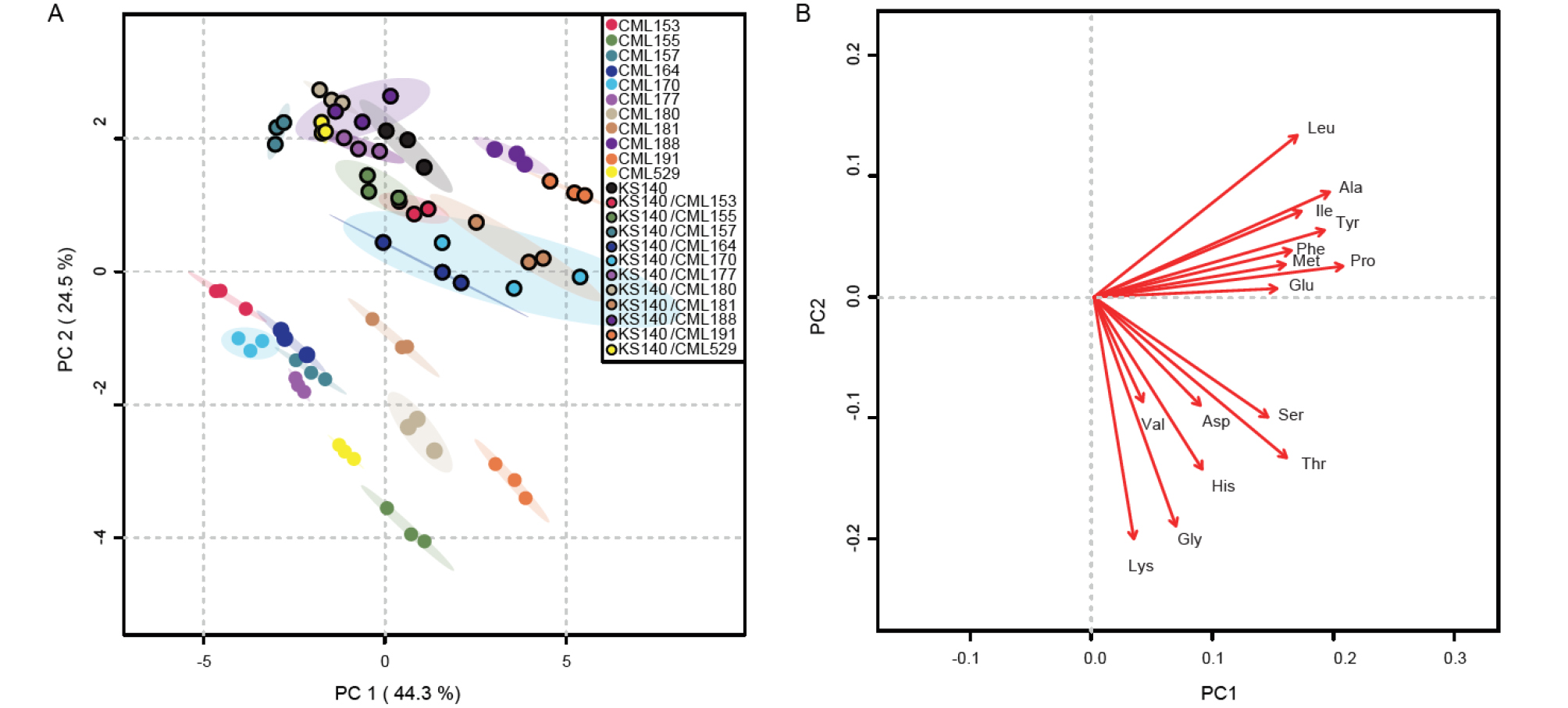
옥수수의 아미노산 조성에 따라 시험 계통들은 크게 두 개 그룹으로 나눌 수 있었으며 CML 계통도 두 개의 그룹으로 나눌 수 있었다(Fig. 1). CML155, 180, 181, 191을 포함하는 Group I은 lysine을 비롯하여 histidine, glycine, threonine, serine의 조성비율이 높으며, CML153, 157, 164, 170, 177을 포함하는 Group II는 이들 조성비가 상대적으로 낮았다. KS140의 경우 valine, methionine, alanine 및 leucine 조성비가 상대적으로 높으며(Table 3, Fig. 1), 교잡계에서도 이와 비슷한 그룹간의 차이를 보였다. Group I에 포함되는 교잡계는 Group II에 포함되는 교잡계에 비해 lysine, threonine, serine의 조성비가 높았다. Group II에 포함되는 CML177은 특이적으로 valine의 조성비가 높았다. 실험 계통 및 교잡계에 대한 특성을 파악하기 위해 아미노산 조성에 따른 주성분 분석(PCA)을 수행하였다. CML 계통들은 score plot의 좌하단에, 교잡계들은 우상단에 위치하여 두 그룹이 뚜렷이 구분되었다(Fig. 2A). Loading plot에서 좌하향으로 lysine이 위치하는 것으로 보아 CML계통과 교잡계의 구분에 lysine이 중요한 역할을 하는 것을 알 수 있었다. 또한 leucine과 alanine은 우상향으로 위치하여 KS140과 교잡계에 조성비가 높음을 알 수 있었다(Fig. 2B). CML188의 경우 KS140 또는 교잡계와 비슷한 곳에 위치하는 것으로 보아 QPM이 아닐 수 있음을 보여준다. 대체로 교잡계들은 모본인 KS140과 더 유사한 아미노산 조성을 보인다고 할 수 있으나, 일부 조합 교잡계에서 아미노산의 조성이 모본이 KS140과 큰 차이를 보이므로 교잡계 혹은 그 후대에서 QPM으로 육성될 수 있는 가능성을 확인하였다. 특히 QPM 원인유전자인 opaque2 유전자형 확인을 통해 선발 효율을 높일 수 있을 것으로 판단된다.
적 요
본 연구는 non-QPM인 KS140, QPM인 CML 계통 및 교잡계의 생육 특성과 단백질, 지방산 등 일반성분, 아미노산 조성을 분석하여 국내 적응 QPM 신품종 육성을 위한 기초 연구 자료로 활용하고자 수행하였다.
1.출사일수는 CML 계통이 78~90일, CML 교잡계가 81~87일 이었고 평균 출사일 수는 KS140, CML 계통 및 교잡계 모두 85일 이었다. CML계통 중 CML191이 간장과 착수고 모두 155 cm, 72 cm로 가장 낮았고, CML529의 간장이 242 cm, CML164의 착수고가 139 cm로 가장 높았다. 과피색은 KS140이 노란색, CML 계통은 흰색과 노란색이었고, 교잡계는 CML 계통이 흰색인 경우에는 노란과 흰색의 중간색을 나타내었다.
2. CML 계통의 단백질 함량은 9.1~12.1% 범위로 CML153이 가장 적었고 CML191이 가장 많았다. CML 교잡계의 단백질 함량은 9.1~11.1% 범위로 KS140/CML170이 가장 적었고, KS140/CML188이 가장 많았다.
3. 지방산의 조성비는 KS140, CML 계통과 교잡계 모두 C18:2 (linoleic acid)가 가장 높았고 C18:1 (oleic acid), C16:0 (palmitic acid), C18:0 (stearic acid), C18:3 (linolenic acid) 순이었다. CML 계통의 평균 포화지방산 비율은 21.4%였으며 불포화지방산 조성비는 78.6%로 KS140보다 포화지방산 조성비가 다소 높았다.
4. 아미노산 조성비 중 KS140, CML 계통 및 교잡계에서 Glutamic acid 함량이 가장 높았으며 lysine의 조성비는 non-QPM인 KS140이 2.51%, QPM인 CML 계통 평균이 4.83%였으며 CML155가 6.92%로 가장 높았다. CML 교잡계 평균은 3.46%였고 KS140/CML164와 KS140/ CML170의 lysine 조성비는 각각 4.18%과 4.99%로 교배하기 전의 QPM계통인 CML164, CML170보다 높았다.
5. 아미노산 조성에 따라 시험 계통들은 크게 두 개 그룹으로 나눌 수 있었으며 CML 계통도 두 개의 그룹으로 나누어졌다. CML155, 180, 181, 191을 포함하는 Group은 lysine을 비롯하여 histidine, glycine, threonine, serine의 조성비가 높았고, CML153, 157, 164, 170, 177을 포함하는 Group은 아미노산 조성비는 상대적으로 낮았다.