서론
재료 및 방법
옥외환경조절시설(SPAR)
옥외환경조절시설(SPAR) 환경
생육조사
무기영양 분석
결과 및 고찰
감자 군락형태 변화
시기별 탄소와 질소 변화
시기별 인산과 칼륨 변화
시기별 칼슘과 마그네슘 변화
시기별 괴경의 단백질 함량 변화
적요
서론
지구 대기중의 이산화탄소 농도는 하와이 마우나로아에서 1959년 315 μmol mol-1로 측정되기 시작한 이래, 2017년 8월 404 μmol mol-1으로 현저하게 증가하고 있는 추세이다. 이와 함께 2017년 온도는 20세기 평균 15.6℃보다 0.83℃ 높아지고 있다(NOAA, 2017). 이러한 지구온난화로인해 가뭄, 홍수와 같은 비생물적 스트레스의 발생 빈도가 높아지면서 작물의 군락형태와 무기영양분에 변화를 주고 있다.
작물의 군락 형성에 있어서 초장과 엽수 그리고 엽면적은 매우 중요한 역할을 하는데 지상부의 환경에 의해 제한적으로 변화를 받는다(Schittenhelm et al., 2006). 식물에 있어서 일반적으로 탄소 농도는 건물에 약 45%를 함유하고 있으며, 상승된 이산화탄소 농도에 따라 식물체내의 탄소와 질소 농도가 바뀐다(Gifford et al., 2000). 무기영양은 작물의 종류와, 근권, 온도, 토양 pH 농도 그리고 토양의 무기성분과 같은 다양한 환경요인 등에 의해 영향을 받는다(Tindal et al., 1990). 최근 기후변화로 비생물적 스트레스의 발생이 높아짐에 따라 식물체 건물 중과 유기물의 합성과 분해와 같은 대사작용에 영향을 주는 식물체 내의 무기영양 함량 변화를 줄 수 있으며, C3 작물 가운데 벼, 보리, 밀, 콩, 감자 등에서 지상부와 지하부의 단백질 함량이 각각14%와 9%가 감소를 하였고(Taub et al., 2008), 밀, 벼 그리고 보리에서 마그네슘, 아연 그리고 철분 함량이 2~20%가 감소를 하였다(Myers et al., 2016).
C3 작물인 감자는(Solanum tuberosum L.) CO2 농도에 따라 광합성효율을 향상시켜 건물중과 수량 증가(Fleisher et al., 2008a; Fleisher et al., 2008b; Högy and Fangmeier, 2009a) 뿐만 아니라 물과 질소 효율성을 향상 시킨다(Kimaball et al., 2002; Fleisher et al., 2013). 감자의 괴경은 양질의 단백질과 칼륨 그리고 마그네슘을 함유하고 있다. 그러나 괴경비대기의 한발은 수량을 저해 시킬 뿐만 아니라 품질에도 영향을 준다(Walworth and Carling, 2002; Rolando et al., 2015). 지난 20년간 FACE와 Open-Top 챔버 등에서 상승된 CO2 농도에 따라 작물의 무기영양 변화에 관한 연구를 수집하여 분석한 결과 감자에 있어서 질소 농도가 감소함으로써 괴경의 단백질 함량이 감소하였으며(Taub et al., 2008; Myers et al., 2016), 작물에 따라 상승된 CO2 농도에 대한 무기영양 농도 변화는 다르지만 질소, 아연 그리고 철분이 감소가 되었다(Ziska et al., 2016). 그러나 Pikki et al. (2007)의 보고에 따르면 상승된 CO2 농도에서 인산, 칼륨, 마그네슘 그리고 칼슘의 변화 하지 않았다는 결과도 있다. 최근 Mcgrath and Lobell (2013)의하면 상승된 CO2농도와 관련하여 자료를 수집한 결과 21개의 무기영양 가운데 17개가 감소하였으며 특히 12개가 매우 유의하게 감소를 하였다.
결국 지구온난화의 가속화에 따른 이상기상 발생은 작물의 군락형태와 무기성분이 비가역적으로 변화되어 작물의 수량과 인간의 단백질 같은 영양 공급에 잠재적인 영향을 줄 것으로 판단된다.
현재까지 연구된 보고는 상승된 온도와 CO2 농도와 온도를 개별적으로 분석하여 최종 수확기에 대한 무기영양 변화를 분석 할 뿐 가뭄과 같은 비생물적 스트레스와 생육 시기에 따른 각각의 조직에 대한 연구는 미미한 실정이다. 따라서 본 연구는 향후 기후변화를 대비하여 자연환경과 유사하게 작물 군락을 형성하여 온도와 CO2 농도 그리고 수분 등을 인위적으로 제어할 수 있는 옥외환경조절시설인(Soil- Plant-Atmosphere-Research: SPAR)챔버(Reddy et al., 2001)에서 상승된 CO2와 온도 그리고 괴경비대기에 한발 스트레스를 재현함으로써 감자의 생육시기의 군락 변화와 잎, 줄기 그리고 괴경의 무기성분 변화를 구명하고자 한다.
재료 및 방법
옥외환경조절시설(SPAR)
본 연구는 국립식량과학원 옥외환경조절시설에서 플렉시 글라스(Evonik Industries, Essen, Germany)재질로 만들어진 챔버(2 m × 0.95 m × 2.25 m: 길이 × 너비 × 높이)로 그 안에 모래 60%, 미사 30% 점토 10%로 구성된 토양 통(2 m × 0.78 m ×1.42 m: 길이 × 너비 × 높이)에 봄 감자의 대표 품종인 수미(Superior)를 파종 하였다. 시비량은 N-P2O5-K2O를 10-8.8-13 kg/10a을 투입하였다. 생육기간 동안 챔버에 CO2센서(LI-820, LI-COR Biosciences, Inc., Lincoln, USA)을 싱글빔으로 2파장 비분산형 근적외선분석계(Non-dispersive infrared: NDIR)로 설치하여 24시간 이산화탄소 흡입과 배출을 측정하였다. 토양 통 안에 토양 수분 함량과 지온을 동시에 측정할 수 있는 FDR (Soil Moisture Sensor, Senkek, Australia)센서를 설치하여 측정하였다.
옥외환경조절시설(SPAR) 환경
상승된 이산화탄소 농도와 온도 그리고 한발에 따른 감자의 군락과 그에 따른 무기영양 변화를 비교하기 위해 Table 1과 같이 챔버 환경을 조절 하였다. 본 시험에 사용된 3 개의 챔버 중 1개는 현재 기후와 유사하게 하여 온도는 전주 30년(1980~2010) 일일 기온 평균에 이산화탄소 농도는 450 μmol mol-1 (ATC450)로 하였고, 다른 2개의 챔버는 RCP 8.5 기후변화 시나리오에 근거하여 온도는 전주 30년 일일 평균 기온 대비 2.8℃를 높이고, 이산화탄소 농도는 700 μmol mol-1 (AT+2.8C700)로 처리를 하였다. 관수는 3~4일 간격으로 챔버 당 약 10~20 L씩 공급 하다가 1개 챔버(AT+2.8C700DS)는 출현 후 40일부터 3주간 한발 스트레스 처리를 하였다. 토양 수분 함량은 Fig. 1과 같이 AT+ 2.8C700DS는 출현 후 45일 이후부터 토양수분 함량이 감소 하다가 출현 후 62일에 재 관수하여 수분 함량이 증가를 하였다.
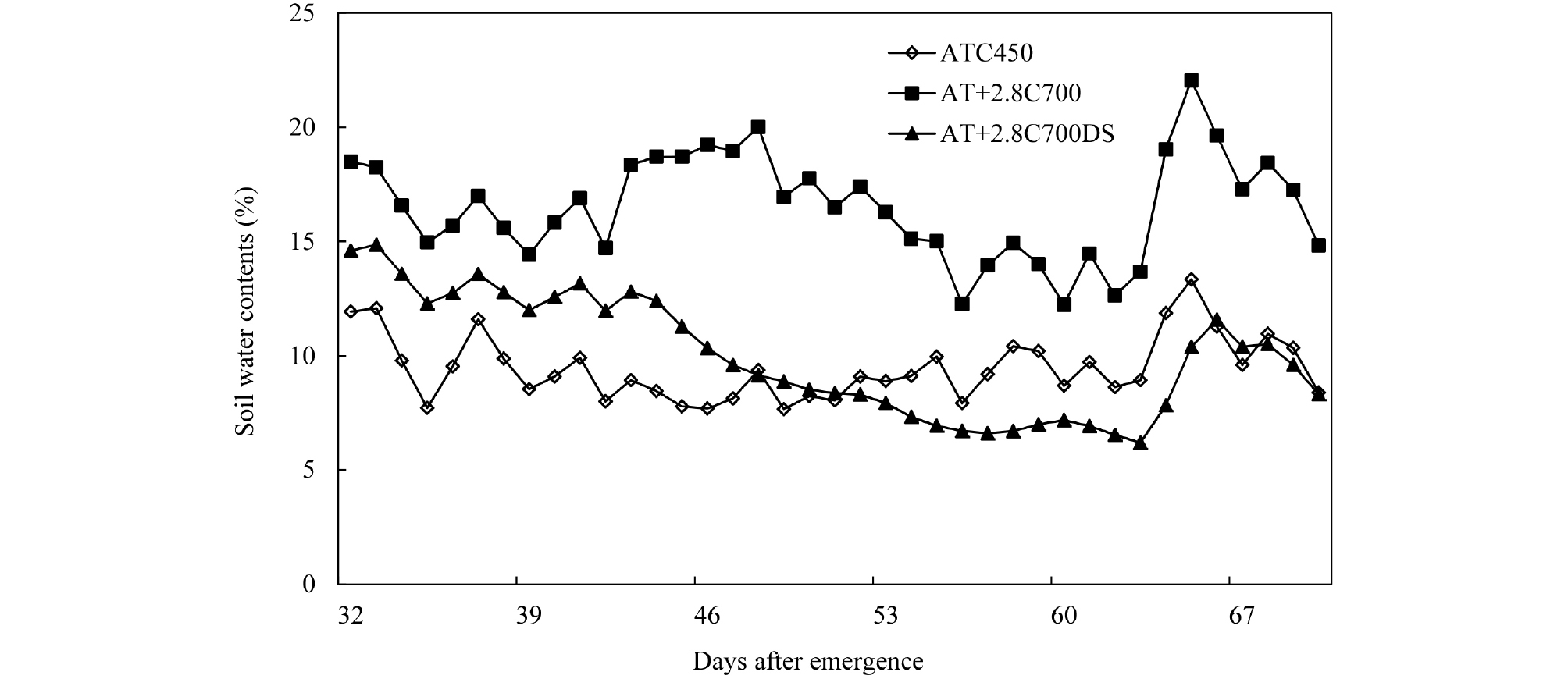
Fig. 1.
Daily average soil water contents during potato plant growth
DAE: days after emergence.
ATC450: 30-year average temperature at 450 μmol mol-1 of CO2
.AT+2.8C700: 30-year average temperature + 2.8℃ at 700 μmol mol-1 of CO2.
AT+2.8C700DS: 30-year average temperature + 2.8℃ at 700 μmol mol-1 of CO2 under drought stress.
생육조사
생육 반응을 비교하기 위해 출현 후 약 30일부터 10~14일 간격으로 수확기까지 엽면적 측정기(LI-3100C, LI-COR, Biosciences, Inc., Lincoln,USA)로 엽면적을 측정하였다. 채취한 식물체를 잎, 줄기 그리고 괴경으로 구분하여 70℃ 항온 건조기에 96시간 건조 후 건물 중을 측정하였다.
무기영양 분석
무기영양 분석은 건조된 잎, 줄기 그리고 괴경을 소형파쇄기로 균일하게 분쇄하여 분석 시료로 사용을 하였다. 탄소와 질소 분석은 N2O를 N2로 환원시켜 N2가스의 부피를 측정하여 정량 하는 Dumas법으로 0.2g씩 칭량 후 원소분석기(Elementary, vario MAX cube., Germany)로 분석을 하였다. 치환성 양이온(P, K, Ca, Mg)분석은 시료 0.5g씩 칭량 후 습식분해 법으로 분해용액(HNO3: H2SO4: HClO4 = 10: 1: 4)을 첨가하여 220℃로 4시간 분해 후 여과과정을 거쳐 분광분석기(UV-Cintra 404, GBC Scientific Equipment Pty Ltd., Australia)로 인산분석을 하였고, 유도 결합 플라즈마 발광광도계(Inductively Coupled Plasma Spectrophotometry Mass, ICP Integra XL, GBC Scientific Equipment Pty Ltd., Australia)를 이용하여 칼륨, 칼슘, 마그네슘을 분석하였다. 단백질 분석은 질소 농도에 단백질 환산 계수 6.25를 곱하여 계산하였다. 생육 시기별 무기영양 분석은 3반복으로 표준오차로 하였다.
결과 및 고찰
감자 군락형태 변화
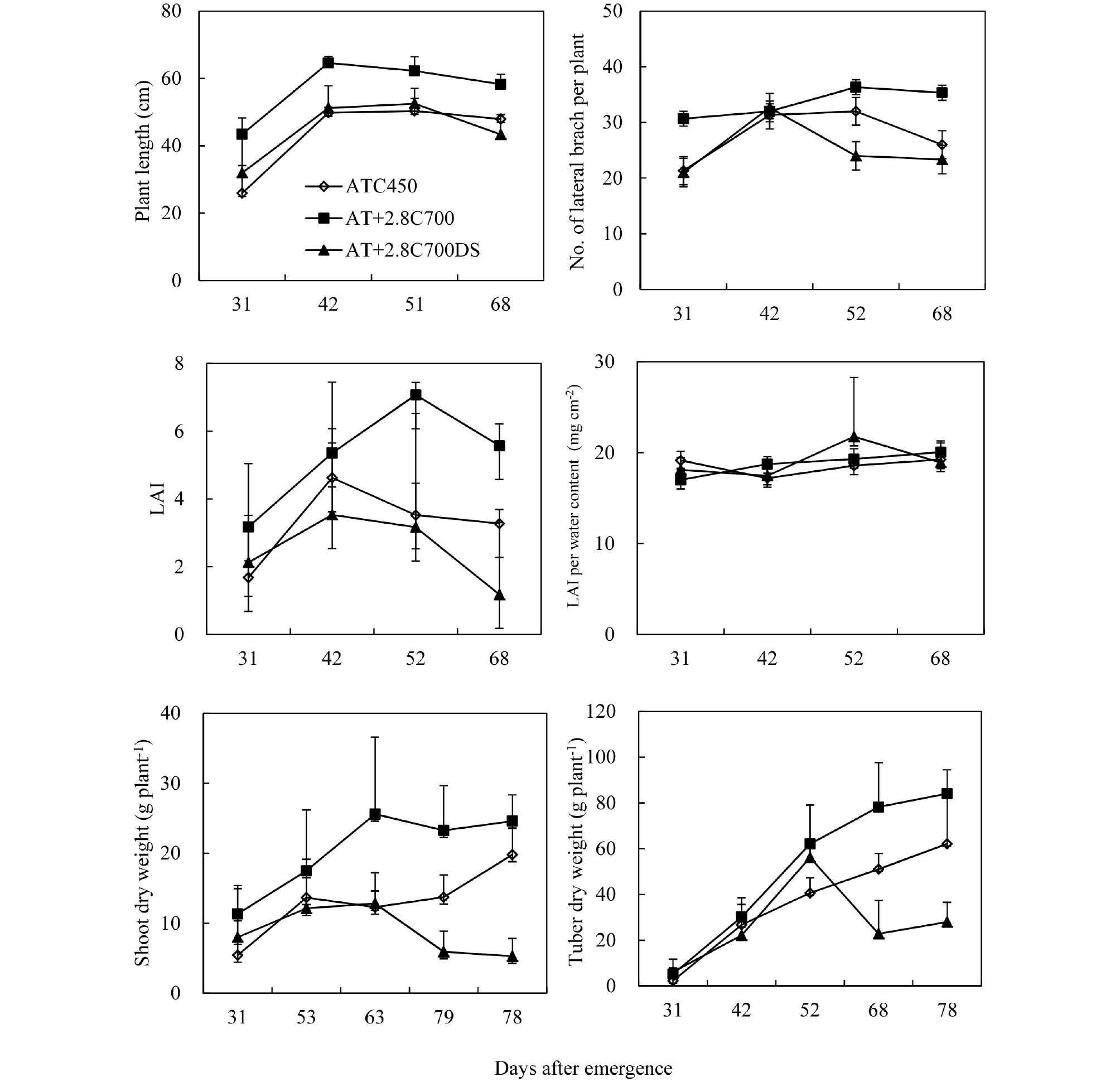
감자 지상부의 초장과 측지수는 군락 형성에 매우 주요한 요소로 생육기간 동안 AT+28C700에서 초장이 가장 높았으나, 출현 후 40일부터 모든 처리에서 증가 하지 않았다(Fig. 2A). 측지수는 AT+28C700가 높은 반면 AT+28C700DS는 출현 후 42일 이후부터 한발의 영향으로 감소를 하였다(Fig. 2B). 엽면적의 최대 증가는 AT+28C700에서 출현 후 52일로 ATC450보다 약 10일 정도 길었으며 AT+28C700DS는 높은 CO2 농도와 평년 온도보다 2.8℃ 높은데도 불구하고, 한발 영향으로 생육 후기에 엽면적이 급격히 감소를 하였다(Fig. 2C). 엽면적 당 함수량은 ATC450과 AT+28C700 간에는 유사한 경향을 보였으며, AT+28C700DS는 출현 후 50일에 엽면적이 최대로 높았지만 그 이후 낮았다(Fig. 2D). 이는 함수량이 증가되면서 가용성 물질의 농도가 상대적으로 낮아지면서 삼투퍼텐셜이 증가된 것으로 판단된다. 지상부의 건물 중은 ATC450은 수확기까지 지속적으로 증가 하였다. AT+28C700은 출현 후 50일에 최대 건물 중을 이었으나 그 이후부터는 낮았고 AT+28C700DS은 한발의 영향으로 45일부터 낮았다(Fig. 2E). 괴경의 건물 중은 ATC450과 AT+28C700에서 수확기까지 지속적으로 증가 하였으나, AT+28C700DS은 출현 후 50일부터 지상부와 유사하게 낮아졌다(Fig. 2F). 이러한 한발은 받은 식물은 잎의 잎은 수분 손실을 줄이기 위해 기공이 닫혀지고 CO2가 들어오고 산소가 나가는 것을 제한하게 되는데, 그 결과 잎의 내부는 CO2 농도가 낮아지고 산소의 농도가 높아지면서 CO2의 고정 능력이 떨어지게 되고(Martin and Ruiztorres, 1992; Chaves et al., 2002), 그 결과 호흡작용이 증가하여 체내 물질의 소모가 커지면서 식물체의 생장, 건물중 그리고 엽면적 등이 감소하여 결국 군락 형성을 저해한다고 보고 하였다(Jefferies, 1995; Flesher et al., 2013). 일반적으로 감자의 생육 적정 온도 범위는 16~20℃인데(Yamaguchi and Spurr, 1964), 본 연구에서 AT+28C700은 생육기간 동안 현재 온도 보다 평균 3.1℃ 높았지만 실제 괴경비대기동안 평균 온도는 19.0℃로 온도 상승에 따른 괴경 형성기와 비대기에 장해를 받지 않은 것으로 판단된다.
시기별 탄소와 질소 변화
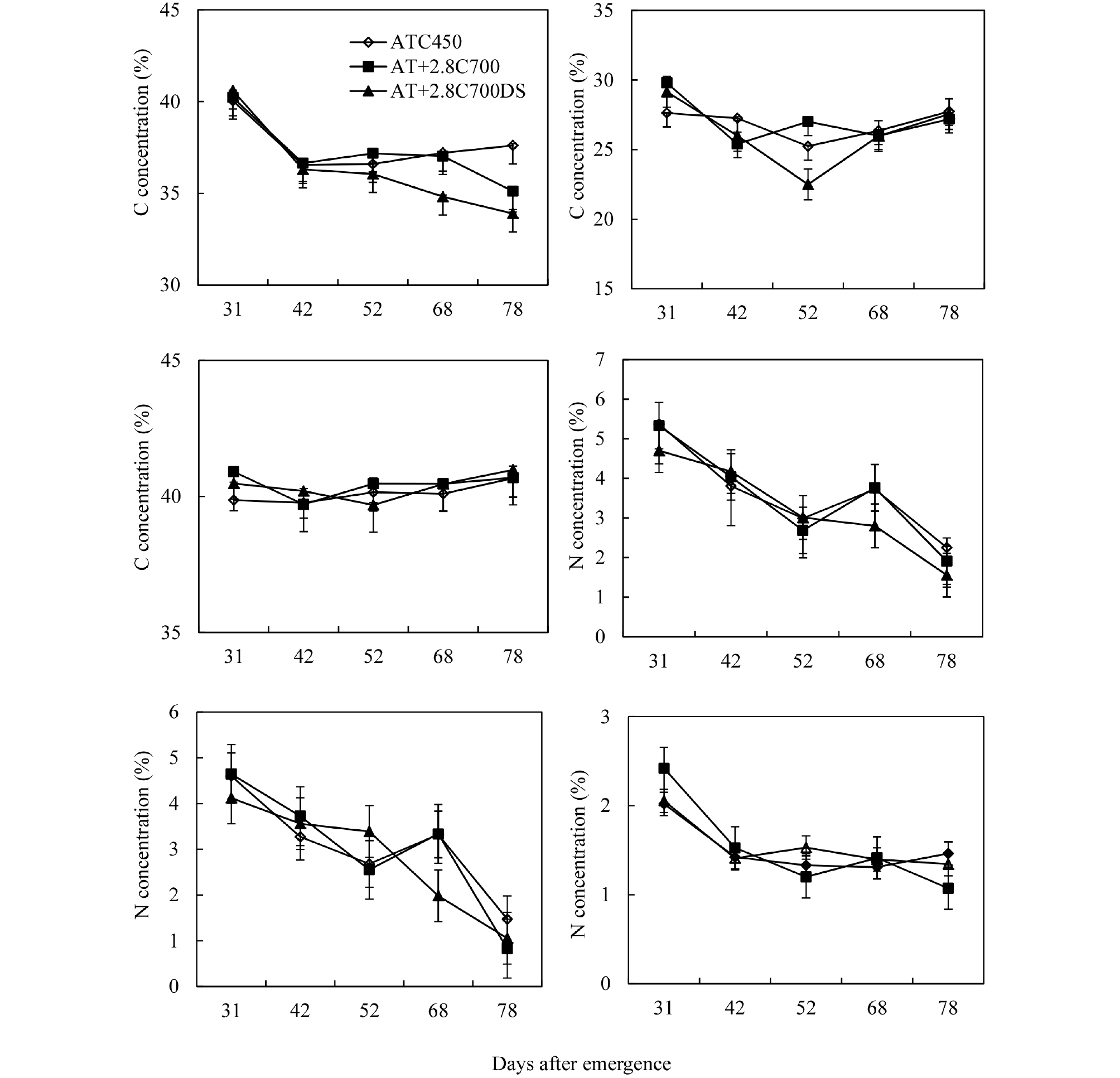
일반적으로 탄소는 작물에 따라서 식물체내에 약 45%를 함유하고 있다. 대기 중의 CO2는 잎의 기공을 통하여 엽육세포로 이동하여 동화물질로 변환하기 때문에 뚜렷하게 잎에서 탄소 변화가 나타난다. 시기별 잎의 탄소 농도 변화를 보면 출현 후 31일과 42일 사이 모든 처리에서 유사하였지만, 수확기인 98일에는 AT+2.8C700이 ATC450에 비해 감소 폭이 증가하여 농도가 낮아졌고, AT+2.8C700DS는 출현 후 50일부터 지속적으로 감소를 하였다(Fig. 3A). 줄기와 괴경은 생육기간 동안 각각 25%와 40% 농도를 유지 하였다(Fig. 3B, C). 질소는 작물생육에 중요한 질소화합물인 아미노산, 단백질, 효소의 구성 성분으로 이들 물질은 광합성에 의하여 동화된 탄수화물에서 합성된다. 일반적으로 질소는 건물 당 약 2~4% 함유되어 있는데, 출현 후 잎과 줄기의 질소 변화는 ATC450과 AT+2.8C700이 유사한 양상으로 변화하였지만, 78일에는 상대적으로 ATC450이 AT+2.8C700에 비하여 감소 폭이 적어져서 농도가 높았다(Fig. 3D, E). Gifford et al. (2000)에 의하면 상승된 CO2 농도에서 식물 조직내의 탄소 농도는 증가하고 질소와 인산 등을 포함한 다른 무기영양분은 감소를 하였다고 한다. 괴경에서는 ATC450이 출현 후 31일 이후 변화 폭이 작은 반면 AT+2.8C700은 ATC450에 비하여 변화 폭이 상대적으로 커지면서 수확기에는 처리들 중 가장 낮아졌다(Fig. 3F).
시기별 인산과 칼륨 변화
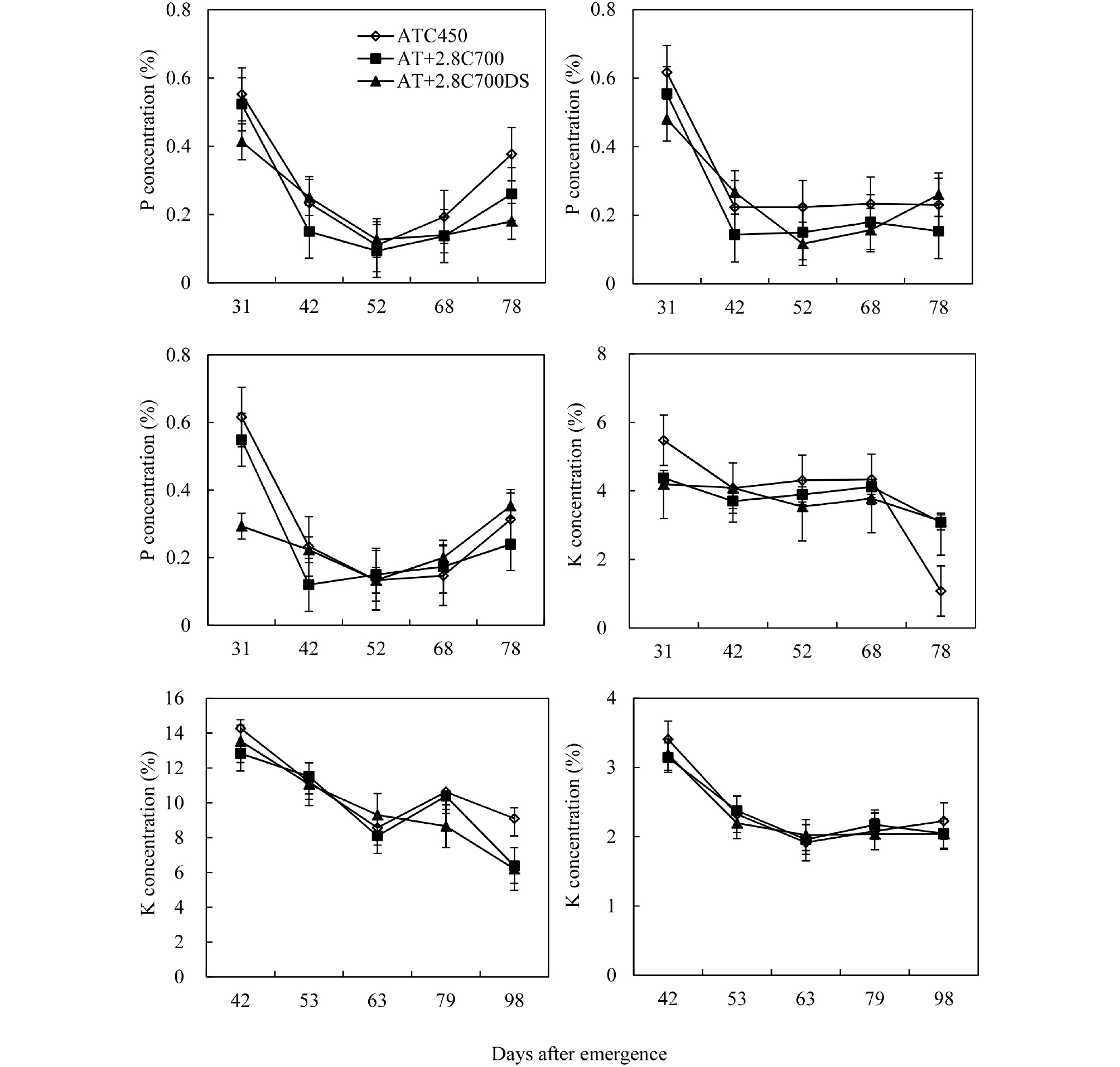
각 처리에 따른 생육기간 동안의 인산 변화는 모든 부위에서 생육 후기로 갈 수록 높아지는 경향을 보였는데, 특히 ATC450이 AT+2.8C700보다 높았다. AT+2.8C700DS는 한발 영향으로 잎과 줄기에서 AT+2.8C700에 비하여 상대적으로 높았다(Fig. 4A, B). Heagle et al. (2003)에 의하면 상승된 CO2 농도에 의해 지상부의 탄소와 질소 농도가 감소를 하였고, 지하부에서는 질소와 인산이 감소를 한다고 보고 하였다. 칼륨의 농도변화는 잎에서는 출현 후 52일부터 AT+2.8C700, AT+2.8C700DS, ATC450 순으로 높았는데(Fig. 4D), 이러한 원인은 AT+2.8C700이 대기 중의 CO2 농도가 높아지면 기공이 닫히고 그로 인해 칼륨 농도가 낮아진 것 판단되며, 한편 AT+2.8C700DS의 잎은 수분을 흡수하려면 공변세포 주변으로 칼륨 농도가 증가하여 기공이 열리지만 한발을 받은 잎은 기공이 닫혀져 칼륨 농도가 상대적으로 낮아져서 삼투압퍼텐셜이 증가 한 것으로 생각된다. 그러나 수확기에는 ATC450이 AT+2.8C700과 AT+2.8C700S비하여 감소 폭이 커지면서 농도가 낮아졌다. 줄기에서는 ATC450과 AT+2.8C700은 비슷한 경향으로 변화를 하였으나, 수확기에는 ATC450보다 AT+2.8C700가 감소 폭이 증가하여 낮아졌다. AT+2.8C700DS는 지속적인 한발로 감소를 하였으나 수확기에는 AT+2.8C700와 비슷한 농도를 보였다(Fig. 4E). 생육기간 동안 괴경은 변화 폭이 적었으나 생육 후기에는 ATC450이 AT+2.8C700보다 약간 높았다(Fig. 4F). Jang et al. (2011)은 국내 감자의 무기영양 중 칼륨이 가장 높다고 하였는데 본 연구와 다소 일치하는 경향을 보였다.
시기별 칼슘과 마그네슘 변화
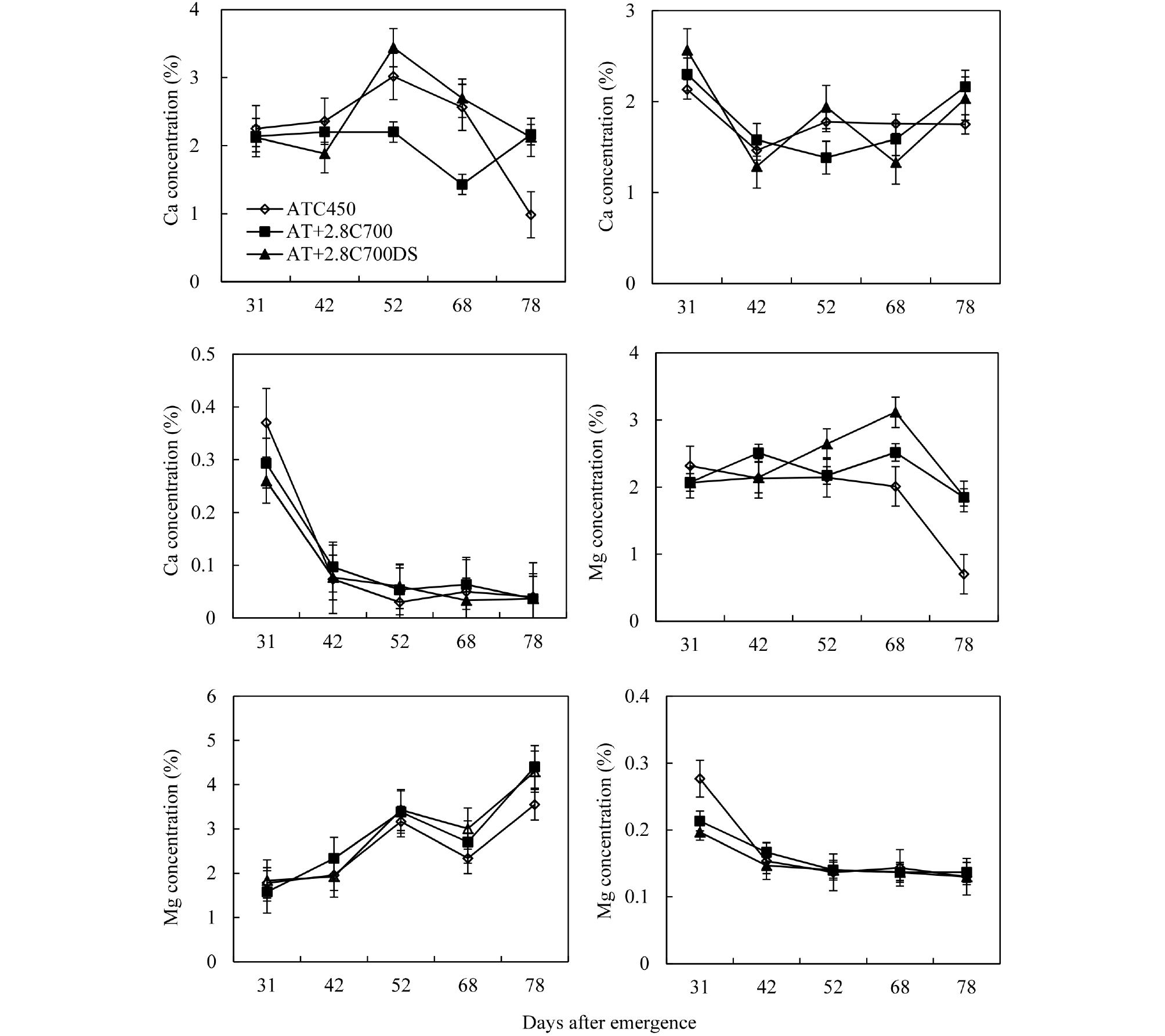
일반적으로 식물체에는 1% 정도의 칼슘이 함유되어 있으며 체내에 이동성이 거의 없다. 칼슘 농도 변화는 잎에서 출현 후 55일 AT+2.8C700DS, ATC450, AT+2.8C700 순으로 높았으나, 수확기에는 ATC450이 감소 폭이 커지면서 AT+2.8C700이 AT+2.8C700DS에 비해 낮았고 AT+2.8C700DS는 한발 발생시 칼슘 농도가 올라가는 경향을 보였으나 생육 후기에는 AT+2.8C700와 비슷하였다(Fig. 5A). 줄기에서는 ATC450이 변화 폭이 크지 않은 반면 AT+2.8C700은 생육 후기로 갈수록 증가 폭이 높아졌다(Fig. 5B). 괴경에서는 생육 후기로 갈수록 칼슘 농도는 감소를 하였다(Fig. 5C). 마그네슘 농도와 관련하여 Mcgrath and Lobell (2013)에 따르면 상승된 CO2의 잎과 줄기에서 마그네슘 농도가 감소 한다고 보고 된바 있다. 그러나 본 연구에서는 생육 후기로 갈수록 잎에서는 ATC450이 농도가 감소를 하였고, AT+2.8C700과 AT+2.8C700DS는 출현 후 68일까지 증가를 보였다. 그러나 AT+2.8C700DS는 한발 발생시 증가 폭이 높아져서 한발을 받지 않은 AT+2.8C700에 비해 증가 폭이 높았다(Fig. 5D). 이러한 결과는 한발 발생시 광합성에 영향을 주는 ATP 감소로 루비스코가 감소하여 마그네슘 농도가 증가 한다고 알려져 있다(Lawlor, 2002). 줄기에서 마그네슘 농도는 잎과 다르게 생육 후기로 갈수록 증가 하였으나, ATC450은 AT+2.8C700보다 증가 폭이 크지 않았다. 그러나 AT+2.8C700DS는 한발의 영향에도 불구하고 AT+2.8C700과 비슷하였다(Fig. 5E). Cao & Tibbitts (1997)에 의하면 CO2농도 상승에 따라 질소, 인산, 칼슘 그리고 마그네슘이 감소를 하였고 칼륨은 변화가 없다고 보고 하였다. 또한 성숙기에 지상부의 질소와 마그네슘 농도가 감소하였고 괴경에서는 질소, 칼륨, 그리고 마그네슘이 감소되었다고 보고 된바 있다(Fangmeier et al., 2002). 또한 Wegener. (2017)에 따르면 한발을 받은 괴경은 11.4~22.2%의 칼슘이 감소를 하였고, 마그네슘과 인 그리고 칼륨은 증가 하였다고 보고 하였다.
시험 결과를 정리하면 상승된 CO2와 온도인 AT+2.8C700는 ATC450에 비하여 지상부에서 질소와 인산이 낮은 반면 칼륨, 칼슘 그리고 마그네슘은 높았다. 괴경에서는 질소, 인산, 칼륨이 낮았으며 칼슘과 마그네슘은 변화가 없었다. 이러한 결과는 질소와 칼륨 그리고 칼슘은 상승된 CO2 농도에 따라 부의 상관관계를 보여준다는 결과와 다소 일치하였다(Högy and Fangmeier, 2009b). 식물체의 무기영양 농도 변화는 근권의 부피 유동과 확산에 따른 변화로 볼 수 있다. 무기영양의 질소, 칼슘, 마그네슘 등은 수용성 다량 원소의 이동 과정으로 토양을 통해 뿌리 쪽으로 이동하여 물에 실려 운반되는데, 뿌리에서 흡수한 대부분의 물은 잎의 기공을 통해 증산을 거쳐 대기로 나가 되면서 불가피하게 광합성을 수행하기 위해 CO2 흡수를 위해 기공이 확산 되면서 물의 소실을 일으켜 무기영양의 변화 가능성을 증가 시킬 수 있다.
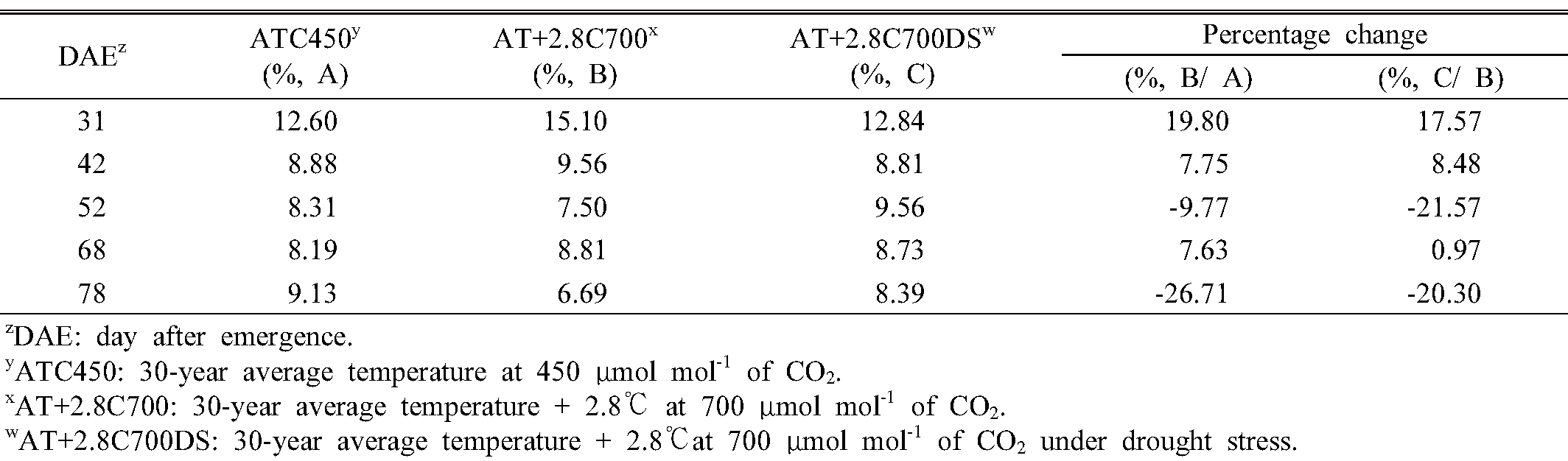
시기별 괴경의 단백질 함량 변화
일반적으로 감자의 단백질 함량은 10% 미만으로 생(Fresh weight)감자에 2%, 건조(Dry weight)된 감자에 7.9%이며 전분 함량에 비하여 낮다고 보고 하였다(Lisska and Leszcyski, 1989; Kolbe and Stefanbeckmann, 1997). 괴경의 시기별 단백질 함량 변화는 Table 2와 같다. 단백질 함량은 출현 후 31일에 AT+2.8C700은 ATC450에 비하여 약 19.8% 높았으나 수확기에는 AT+2.8C700가 ATC450보다 약 26.7% 낮아졌다. 이러한 결과는 FACE와 Open-Top챔버에서 상승된 CO2 조건에서 수확된 괴경의 단백질 함량이 8~24% 감소를 한다는 연구와 일치 하였으며(Donnelly et al., 2001; Tabu et al., 2008; Mcgrath and Lobell, 2013), 이러한 메커니즘은 상승된 CO2 농도에 따라 잎에서 동화물질의 체적으로 인한 광합성 억제와 함께 루비스코의 함량이 감소하면서 C/N률의 변화라고 하였다(Gifford et al., 2000; Ainsworth & Long, 2005). 단백질 함량의 변화는 감자 뿐만 아니라 밀, 보리, 벼, 콩 등에서도 감소 되었다고 한다(Tabu et al., 2008). 한발과 한발을 받지 않은 AT+2.8C700과 AT+2.8C700DS를 비교하면 한발을 받은 AT+2.8C700이 약 20.3%의 단백질 함량이 감소하였는데, 이는 Wegener et al. (2017)에 의하면 한발을 받지 않은 괴경이 한발을 받은 괴경 보다 26~ 30%의 단백질 함량이 증가 하였다고 한다. 따라서 지구온난화에 따른 감자 괴경의 무기 영양인 성분 함량이 변화 될 것이며, 향후 상승된 CO2 농도에 의해 단백질 함량이 감소하게 된다면 인간의 단백질 섭취에 변화를 줄 것이다.
적요
본 연구는 옥외환경조절 시설인 SPAR챔버에서 향후 기후변화가 지속 될 경우 상승된 이산화탄소와 온도 그리고 한발에 따른 감자의 군락 형태와 무기영양 변화에 대한 결과는 다음과 같다.
1.AT+2.8C700는 상승된 CO2와 고온에 의하여 초장과 엽면적 그리고 건물중이 상당히 증가 하였고, AT+2.8C700DS는 한발의 영향으로 상당히 감소하였다.
2.수확기에서 잎은 AT+2.8C700은 ATC450에 비하여 질소와 인산이 감소한 반면 칼륨, 칼슘 그리고 마그네슘 농도가 증가하였다. 괴경은 질소, 인산 그리고 칼륨이 감소하였으며, 칼슘과 마그네슘은 변화가 없었다. 반면, AT+2.8C700DS는 한발의 영향으로 무기영양 농도가 상대적으로 다른 처리비하여 낮았지만, 마그네슘 농도만 증가하였다.
3.CO2와 온도 상승을 보면 AT+2.8C700는 ATC450에 비하여 질소 농도의 감소로 26% 단백질 함량이 감소를 하였다. 한발을 받은 AT+2.8C700DS보다 AT+2.8C700는 단백질 함량이 20%가 감소하였다.
4.따라서 상승된 CO2 농도와 한발은 무기영양의 변화뿐만 아니라 광합성 관련된 당과 아미노산 같은 2차 대사물질도 변화와 인간의 단백질 섭취에도 영향을 줄 것이다.