서론
수수(Sorghum bicolor L. Moench)는 식물학적으로 화본과(Poaceae)에 속하는 일년생식물로 온도가 높고 광이 강한 열대아프리카가 원산지이고, 열대 및 아열대 기후지역에서 많이 재배되고 있다(Kim et al., 2006). 열대 기후에 잘 적응하는 이유는 줄기와 잎의 표면에 얇은 왁스층이 발달되어 있고 잎의 상부표면에 중륵을 따라 기동세포가 발달되어 있어 건조 시 급속히 잎을 말아 수분증산을 억제하기 때문이다. 또한, 요수량은 400 ~ 500 g로 콩 절반 수준이고, 뿌리는 심근성으로 흡비력과 한발 스트레스에 대한 내한성(耐旱性)이 강한 형태적 특성을 지니고 있기 때문이다(Chang et al., 2005).
세계적으로 수수의 생산량은 3,785만 ha에서 55,654천 톤으로 옥수수, 벼, 밀 및 보리 다음으로 많으며, 아프리카가 재배면적의 60%, 생산량의 40%를 점유하고 있다. 우리나라에서 수수의 재배면적과 생산량은 2009년 기준 약 1,500 ha에서 26,000톤이 생산되어 다른 식량 작물에 비해 생산량은 많지 않으나 꾸준하게 생산되는 작물이다. 그러나 최근 들어 건강과 웰빙에 대한 소비자의 관심이 커지면서 다양한 건강 기능성 성분을 지닌 수수의 소비량은 점차 증가할 것으로 보인다.
이상기후 변화에 따른 지구 온난화가 급속하게 진행되면서 우리나라도 온대에서 아열대성 기후로 점차 변화하는 추세이며, 세계적으로 사막 면적은 확대되고 있다(Fraedrich et al., 2001; Beck et al., 2006). 이러한 사막화로 인해 100개국 이상에서 10억 이상의 사람들이 물 부족과 식량부족, 황사 등의 위협에 직면할 것이다(WMO, 2005). 이러한 기후지역에서 상대적으로 한발 적응성이 큰 수수를 재배하고 있지만(Ejeta & Knoll, 2007), 기후변화의 영향으로 수수의 생산량은 2050년까지 현재보다 17%가 더 감소할 것으로 전망되어진다(CGIAR, 2013).
최근 기후변화에 따른 환경 스트레스 하에서 작물의 반응에 대한 연구가 활발하게 진행되고 있으며 과산화수소를 처리하여 여름철 시설 오이의 수분 스트레스와 내서성 증진에 효과가 있으며(Woo et al., 2006), 시설 오이의 고온 적응성 향상에 효과가 있다고 보고되었다(Woo et al., 2005). 몇몇 식물에 과산화수소를 적용하면 항산화와 막지질에 대한 과산화반응의 결과로 열, 저온, 염해와 같은 스트레스에 대한 내성을 증가시킨다고 보고되었다(Uchida et al., 2002; Azevedo Neto et al.; 2005; Wahid et al., 2007). 본 연구는 건조한 지역에서 많이 재배되는 수수에 과산화수소 처리를 통한 한발 스트레스 완화 정도를 알아보고 내한성을 증진시키기 위한 적정 과산화수소 처리방법을 알아보고자 실시하였다.
재료 및 방법
발아실험
공시재료로 2004년 국립식량과학원에서 육성된 조숙이면서 다수성인 황금찰수수를 이용하였다. 수수 종자를 직경 100 mm petri dish에 30립씩 3반복으로 치상하고, 수분 스트레스 처리는 PEG 6000 (polyethylene glycol 6000)을 이용하여 수분퍼텐셜을 0, -0.05, -0.10, -0.15, -0.20 MPa로 조절하였다(Michel & Kaufmann, 1973). 과산화수소 처리는 PEG 6000을 녹인 용액에 10 mM 씩 첨가하여 종자에 처리하였다. 온도는 12시간을 주기로 주야 25℃/20℃로 조절하였으며, 치상 후 2일부터 7일까지 발아조사를 실시하였다. 발아기준은 백체의 길이가 1 mm 이상으로 하였다. 유아와 유근 길이는 치상 후 7일째에 5반복으로 조사하였다.
온실 유묘 실험
2012년은 5월 29일에 유리 온실에 파종하고, 6월 11일 2 kg 사양토를 채운 20 × 20 cm pot에 3주씩 5반복 이식하였다. 수분 처리는 크게 적습과 한발 처리로 나누고, 적습 처리는 토양수분 함량을 30% 내외로 유지하였다. 한발 처리는 이식 2주 후부터 토양수분 함량을 10% 내외로 유지하였다. 한발 처리는 다시 세 가지 처리로 나누었다. 첫 번째는 순화 처리(1주간 한발, 1주간 재관수 후 한발), 두 번째는 한발 1일 전 증류수 엽면처리(한발+H2O), 세 번째는 한발 1일 전 10 mM 과산화수소 엽면처리(한발+H2O2)로 나누어 실험을 진행하였다.
토양 수분퍼텐셜 실험
황금찰수수를 2015년 7월 1일 교내 온실에 파종하고, 7월 14일 0.5 kg 사양토의 밭 토양을 채운 12 cm (H) × 10 cm (D) pot에 2주씩 5반복으로 정식하였다. 정식 5일 후 PEG 용액을 관수하여 토양의 수분퍼텐셜을 0 MPa, -0.05 MPa, -0.10 MPa, -0.15 MPa, -0.20 MPa로 조절하였다. 정식 7일 후 인 7월 21일에 무처리는 증류수를 엽면처리 하였고 과산화수소 처리는 10 mM 농도로 엽면처리 하였다.
생육 조사는 초장, 줄기 직경, 지상부 건물중, 뿌리 길이 및 지하부 건물중을 조사하였다. 생리적 조사는 잎의 수분퍼텐셜과 수분 함량을 조사하였고, 광합성능력을 알아보기 위해 엽록소함량, 엽록소형광 및 기공전도도를 측정하였다. 수분퍼텐셜은 수수 잎을 1 cm × 1 cm로 잘라 5 g 정도를 용기에 넣고 dewpoint potential meter (WP4-C, Decagon, Pullman, Washington, USA)를 이용하여 측정하였다. 지상부와 지하부의 수분 함량은 생체중에서 건물중을 뺀 값을 이용하였다. 엽록소함량은 휴대용 엽록소계(SPAD-502, Minolta, Osaka, Japan)을 이용하여 상위 3번째 잎의 중간부위를 10반복으로 조사하였으며, 엽록소형광은 chlorophyll fluorometer (OS-30p, Opti-sciences, Hudson, NH, USA)를 이용하여 엽록소함량을 조사한 부위에 광차단 클립으로 20분간 암처리 후 3반복 측정하였다. 기공전도도는 엽록소함량과 형광을 조사한 동일한 잎을 대상으로 leaf porometer (SC-1, Decagon, Pullman, Washington, USA)를 이용하여 3반복 조사하였다.
통계 분석
각 실험 별로 얻어진 데이터는 SAS 프로그램(ver. 9.3. Cary, USA)을 이용하여 PROC ANOVA로 분산분석을 실시하고 던칸다중범위검정법(Ducan’s multiple range test, DMRT)을 통해 평균값 p < 0.05 유의수준에서 비교하였다.
결과 및 고찰
발아반응
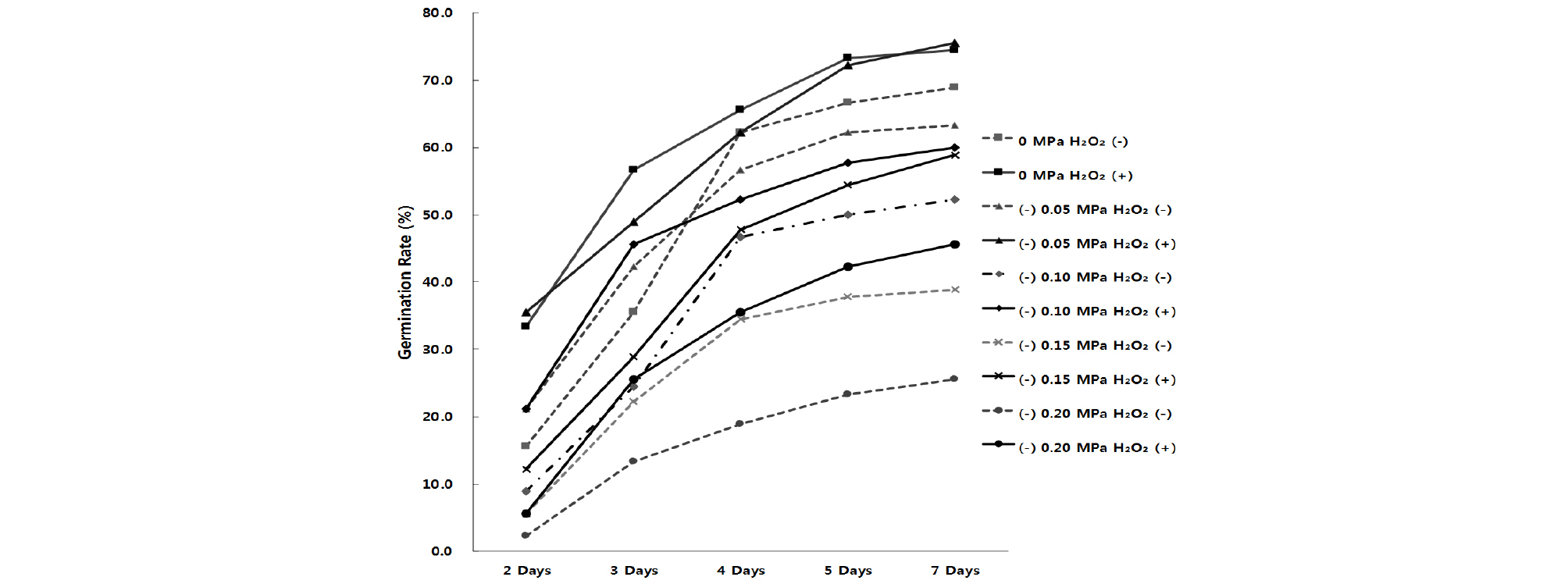
과산화수소는 여러 식물종에서 종자 발아를 촉진하는 효과가 인정되었고 밀을 통한 예비실험에서 과산화수소 농도별(1, 10 및 100 mM)로 처리하면 DPPH의 라디칼 소거능이 10 mM에서 가장 높게 측정되었다. 최소 1 mM에서 최대 30 mM의 과산화수소를 처리한 연구 결과 등을 바탕으로 최적농도로 10 mM로 설정하여 과산화수소를 처리하였다. 과산화수소 처리가 수분 스트레스 하에서 수수의 발아에 미치는 영향을 보면, 과산화수소 처리가 0 MPa를 포함한 모든 수분 스트레스 조건(-0.05 ~ -0.20 MPa) 하에서 발아율이 향상되는 결과를 보였다(Fig. 1). 처리 7일차 발아율은 0 MPa 조건에서 과산화수소 처리 시 발아율 증가가 5.5%로 발아율의 차이가 가장 낮았으며, 수분 스트레스가 가장 심한 -0.15 MPa와 -0.20 MPa에서 과산화수소 처리에 의한 발아율 증가가 20.0%로 발아율의 차이가 가장 크게 조사되었다(Fig. 1). 이는 과산화수소가 발아 과정에서 자극을 주어 대사 활성을 유도하여 수분 스트레스가 심한 조건에서 발생하는 대사 저하를 완화하였기 때문으로 보인다(Gregorio et al., 2012).
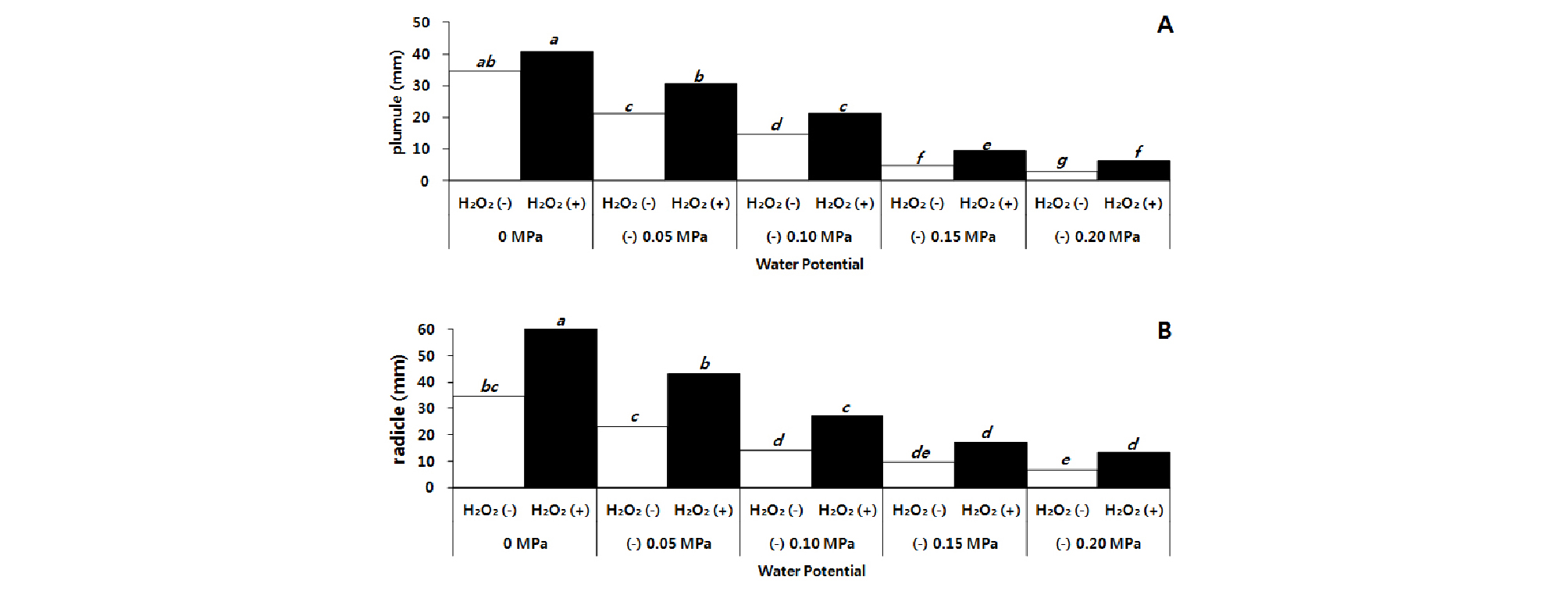
유아와 유근의 길이를 조사한 결과, 발아 속도가 빠르고 발아율이 우수하였던 과산화수소 처리에서 증류수 처리보다 유아, 유근의 길이 신장이 촉진된 것을 알 수 있었으며, 수분 스트레스가 증가할수록 유아, 유근의 길이 신장이 저해되는 것을 알 수 있었다(Fig. 2). 수분 스트레스 증가는 강낭콩(Phaseolus vulgaris L.)에서 광합성 색소, 총 탄수화물 및 식물호르몬을 크게 감소시켜 발아와 초기 생육을 저해 하지만 과산화수소를 종자에 전처리하면 종자 내 항산화 물질의 활성화를 유도하여 수분 스트레스로 인한 식물 생장의 생리학적 특성을 향상시키고 산화 손상을 완화하여 발아 및 초기 생육을 촉진하였다(Abass & Mohamed, 2011).
Gregorio et al. (2012)에 의하면 활성산소종은 종자 발아 과정에 부정적인 영향을 줄 수 있으나 활성산소종 생성과 소거 사이의 균형이 엄격히 조절된다면 이러한 독성 라디칼은 종자 발아에 유익하게 작용할 수 있으며 활성산소종인 과산화수소를 처리하게 되면 종자의 수분 흡수를 활성화하여 발아뿐만 아니라 유아와 유근의 성장을 증가시킨다고 보고하였다.
과산화수소 처리는 호르몬 수치를 조절하여 종자 발아가 유도 될 수 있는 분자신호로 작용하는 등 종자 프라이밍 기술에 많이 이용되어 활력이 적은 종자의 활성화에도 이용되고 있다. 종자 발아 증진을 위해 다양한 물질의 효과에 대한 실험이 이루어졌으나, 과산화수소를 제외한 GSH (oxidized glutathione), ASC (ascorbic acid), OTC (L-2-oxo-4-thiazolidine-carboxylic acid), NAC (N-acetylcysteine), TP (thioproline), SA (salicylic acid), BTH (benzothiadiazole) 등의 화합물은 종자 발아에 영향을 주지 못하였으며, 10 ~ 20 mM 과산화수소 처리에서 정상묘의 발아가 유도 되었으나, 40 mM, 100 mM에서는 비정상묘 출현빈도가 높았다는 보고가 있다(Gregorio et al., 2012). 또한 6 ~ 10 mM 과산화수소 처리는 토마토 종자의 발아율을 높였으나 10 mM을 초과할 경우 유아 및 유근의 손상을 초래하여 농도 별로 그 효과가 상이하게 나타난다(Lu & Higgins, 1999). 따라서 식물 종자 상태에 따른 적절한 과산화수소 적용 농도의 기준 마련에 대한 추가 연구가 필요하다.
수수 Pot 유묘 실험
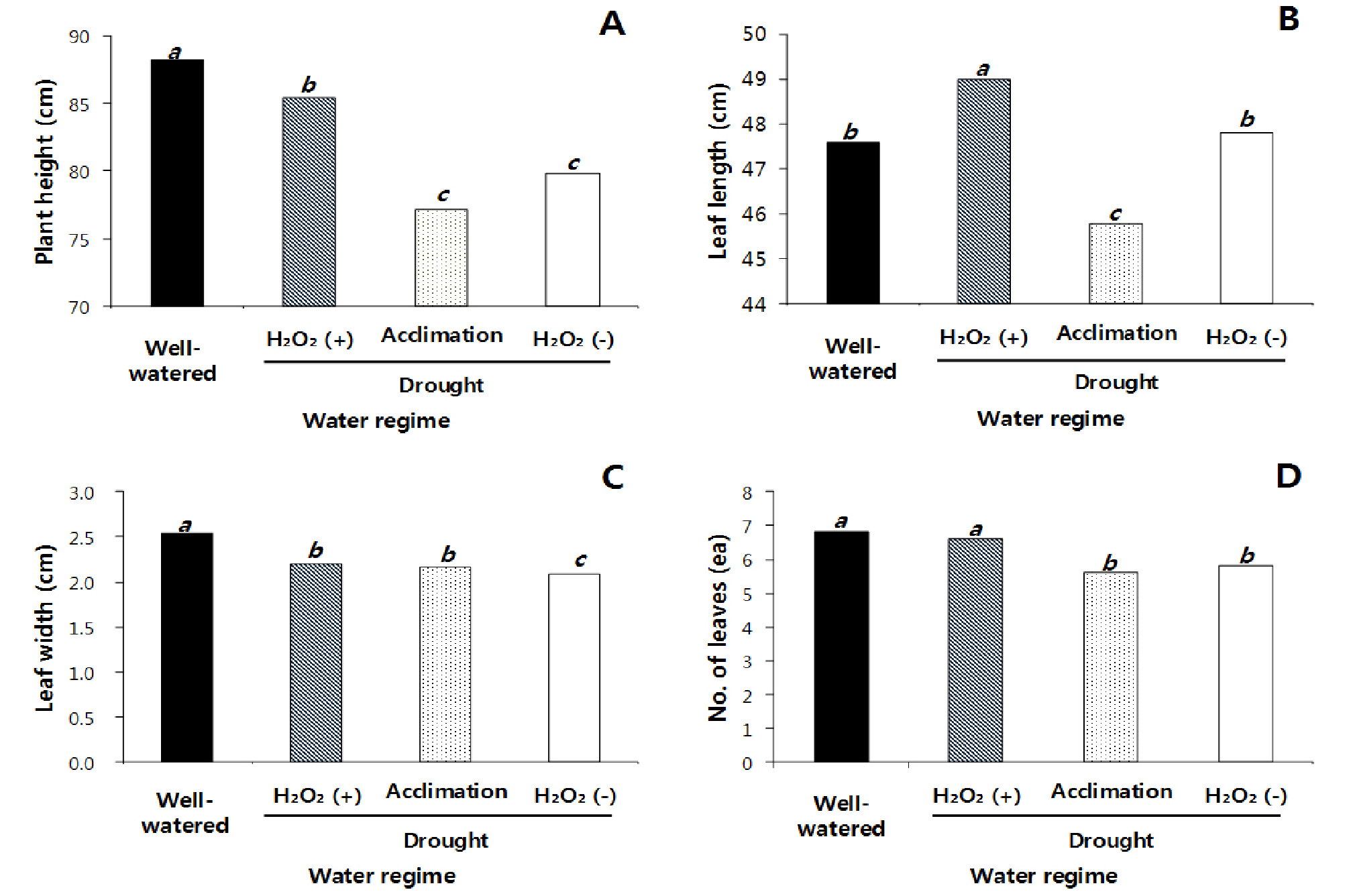
2012년 온실 pot 실험의 결과는 적습 처리에서 전체적으로 생육이 우수하였다. 처리 2주 후 초장을 보면, 적습 처리에서 88.2 cm로 가장 컸으며, 한발+H2O2 처리에서 적습 조건 대비 3.2% 감소한 반면, 한발+H2O 처리 및 순화 처리는 적습 처리 대비 각각 9.5, 12.5% 감소한 결과를 보였다(Fig. 3A). 엽장은 한발+H2O2 처리에서 적습 처리 대비 2.9% 증가하였으며, 한발+H2O 처리는 적습 처리 대비 0.4% 증가로 동일한 수준을 보였고, 순화 처리는 적습 처리 대비 3.8% 감소하였다(Fig. 3B). 엽폭은 적습 처리에서 2.54 cm로 가장 넓었고, 한발+H2O2 처리, 순화 처리, 한발+H2O 처리에서 각각 13.4%, 15.0%, 18.1% 감소하였다(Fig. 3C). 엽수는 적습 처리와 한발+H2O2 처리에서 6.8개, 6.6개로 유사하였고, 순화 처리와 한발+H2O 처리에서 1개 적은 5.6개와 5.8개의 엽수를 보였다(Fig. 3D).
상대적으로 순화 처리에서 생육은 다른 한발+H2O2처리, 한발+H2O 처리 보다 낮은 결과를 보인 이유는 예비 한발을 준 7일간 생육이 상대적으로 다른 처리 보다 저조하였기 때문으로 판단된다. 몇몇 식물 종에서 과산화수소 처리는 산화 방지 및 과산화 작용에 의한 순화(경화)됨으로 열, 염, 온도, 한발 스트레스의 내성을 증가 시킨다고 보고되었으며, 기공 폐쇄를 현저히 감소시키고 엽육 세포의 팽창 압력을 유지하는데 기여한다(Bosabalidis & Kofidis, 2002). 결국 한발 스트레스로 유도되는 기공 폐쇄 및 광합성 감소를 줄여 식물체의 영양생장을 유지 시켜준다(Yordanov et al., 2000). 옥수수에서 과산화수소를 염 스트레스 전에 처리하게 되면 처리 15일 차의 지상부 건물중, 지하부의 건물중 및 엽면적의 감소율을 각각 23, 15, 24% 줄여주는 효과가 있으며, 이는 과산화수소 처리된 모든 잎에서 SOD 활성을 증가하여 내염성을 증진시켜 건물량과 엽면적의 감소를 줄여준 것이라고 보고되었다(Azevedo Neto et al., 2005). 1,000 mM 이상의 고농도의 과산화수소는 벼 유묘의 성장 억제를 유발하지만, 저농도의 처리는 100 mM NaCl를 처리한 염 스트레스 하에서 벼 유묘에서 1.3배의 초장 증가 등 생육을 개선하는 효과가 있었다(Uchida et al., 2002). 루핀(Lupinus angustifolius L.)은 한발 스트레스 하에서 뿌리 신장은 무처리 대비 79%로 한발 조건에서 근계 발달이 저하 되어 양분 및 수분 흡수가 저해되어 초장이 무처리 대비 63% 감소하는 등 생육이 저해된다고 알려져 있다(Egamberdieva et al., 2016).
수수 잎의 광합성 관련 능력을 알아보기 위해 수행된 엽록소형광, 엽록소함량(SPAD), 기공전도도 결과를 보면 우선 엽록소형광 값은 적습 처리에서 가장 높았다. 한발+H2O2 처리와 순화 처리가 적습 처리 대비 4.2% 동일한 감소를 보였다. 한발+H2O 처리가 적습 처리 대비 5.6% 가장 큰 감소를 보였다(Fig. 4A). SPAD 값은 적습 처리에서 가장 높았고 순화 처리 2,1%, 한발+H2O2 처리 18.7%, 한발+H2O 처리 38.0%로 적습 처리 대비하여 감소하였다(Fig. 4B). 기공전도도는 적습 처리에서 가장 높았고, 순화 처리, 한발+H2O 처리, 한발+H2O2 처리에서 각각 적습 처리 대비 76.9%, 68.9%, 49.6% 감소하였다(Fig. 4C). 순화 처리가 한발+H2O2 처리 보다는 생육이 다소 부진하지만 광합성능력에서는 유사하거나 높았고, 한발+H2O 처리 보다는 광합성능력이 우수하였다. Pandolfi et al. (2012)은 콩에서 100 mM NaCl 처리 전 25 mM NaCl을 처리하여 순화시키면 SPAD는 11.7%, 기공전도도는 30.4%의 회복율을 보였고, 근계 발달 및 수분 함량은 순화 처리한 것이 무처리 및 염 스트레스 처리 보다 우수하였다. 콩, 완두, 벼, 수수 등에서 저농도의 염 스트레스에 노출되면 스트레스 내성이 향상되어 순화 처리 효과를 나타낸다고 알려져 있다(Ali et al., 2006, Djanaguiraman et al., 2006, Pandolfi et al., 2012).
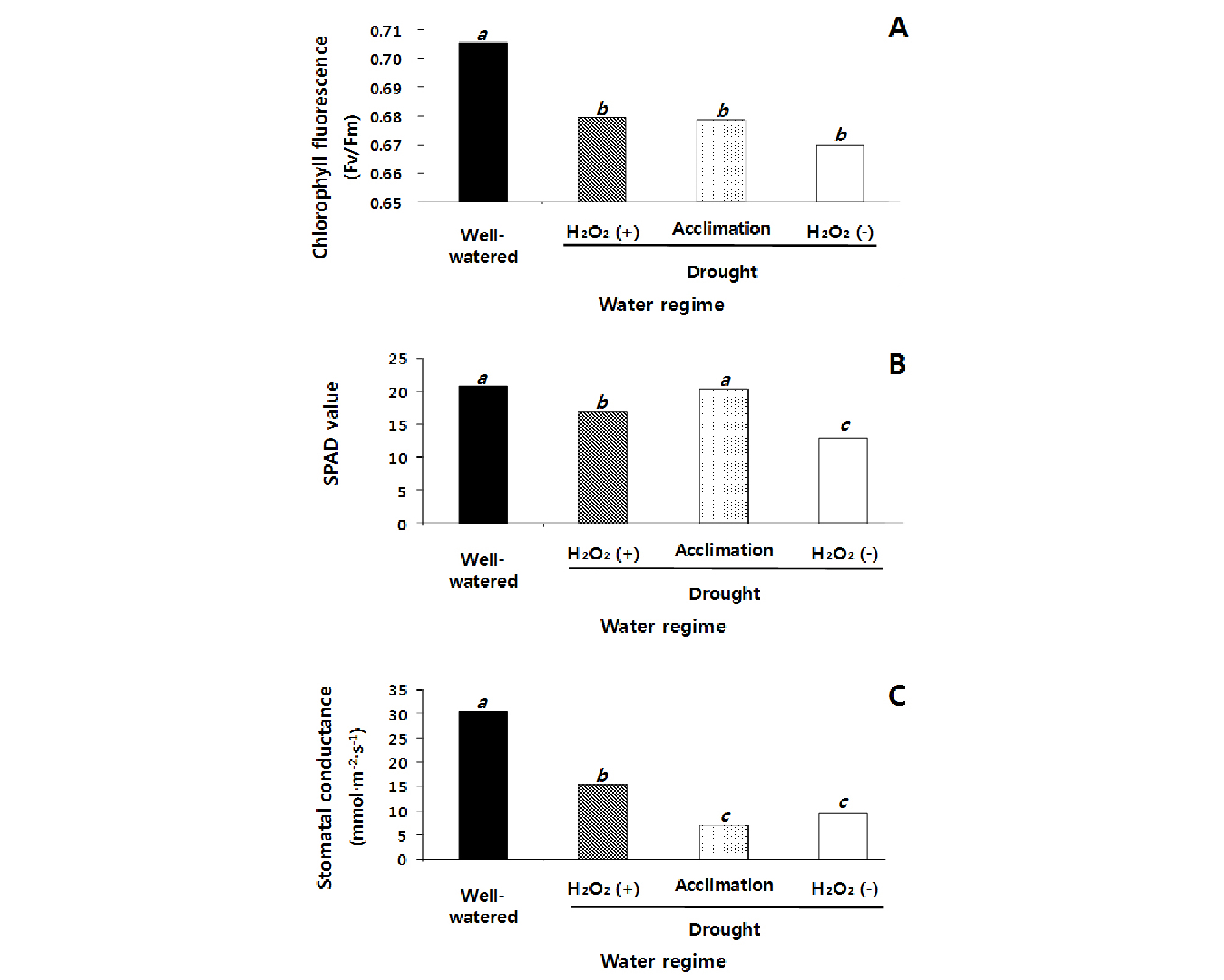
Fig. 4.
Influences of soil water regime and foliar application of H2O2 on chlorophyll fluorescence (A), SPAD value (B) and leaf stomatal conductance (C) of sorghum plants at 2 weeks after drought treatment. The different letters show significant difference (P < 0.05) as determined by Duncan’s multiple range test.
토양 수분퍼텐셜에 따른 수수 반응
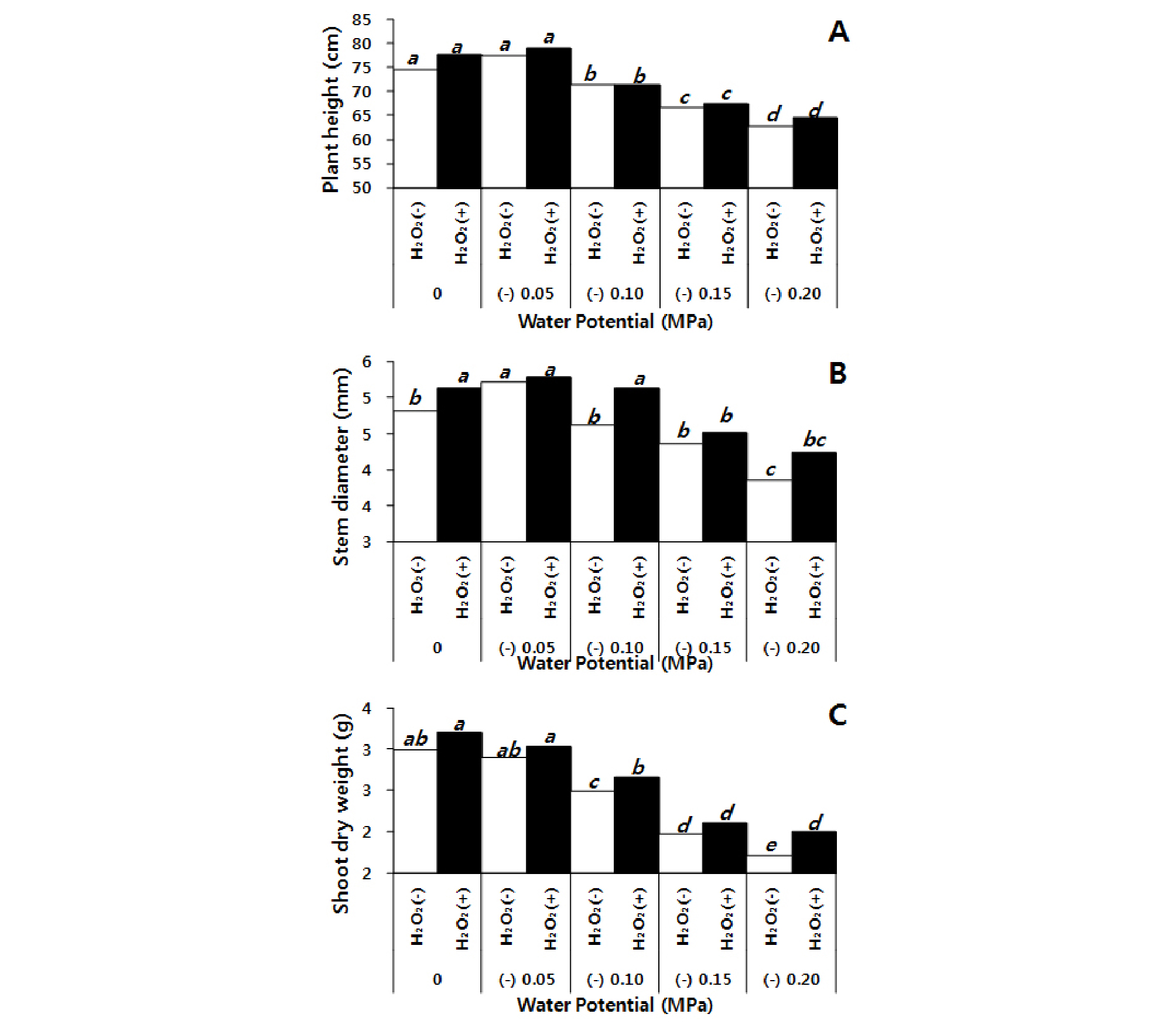
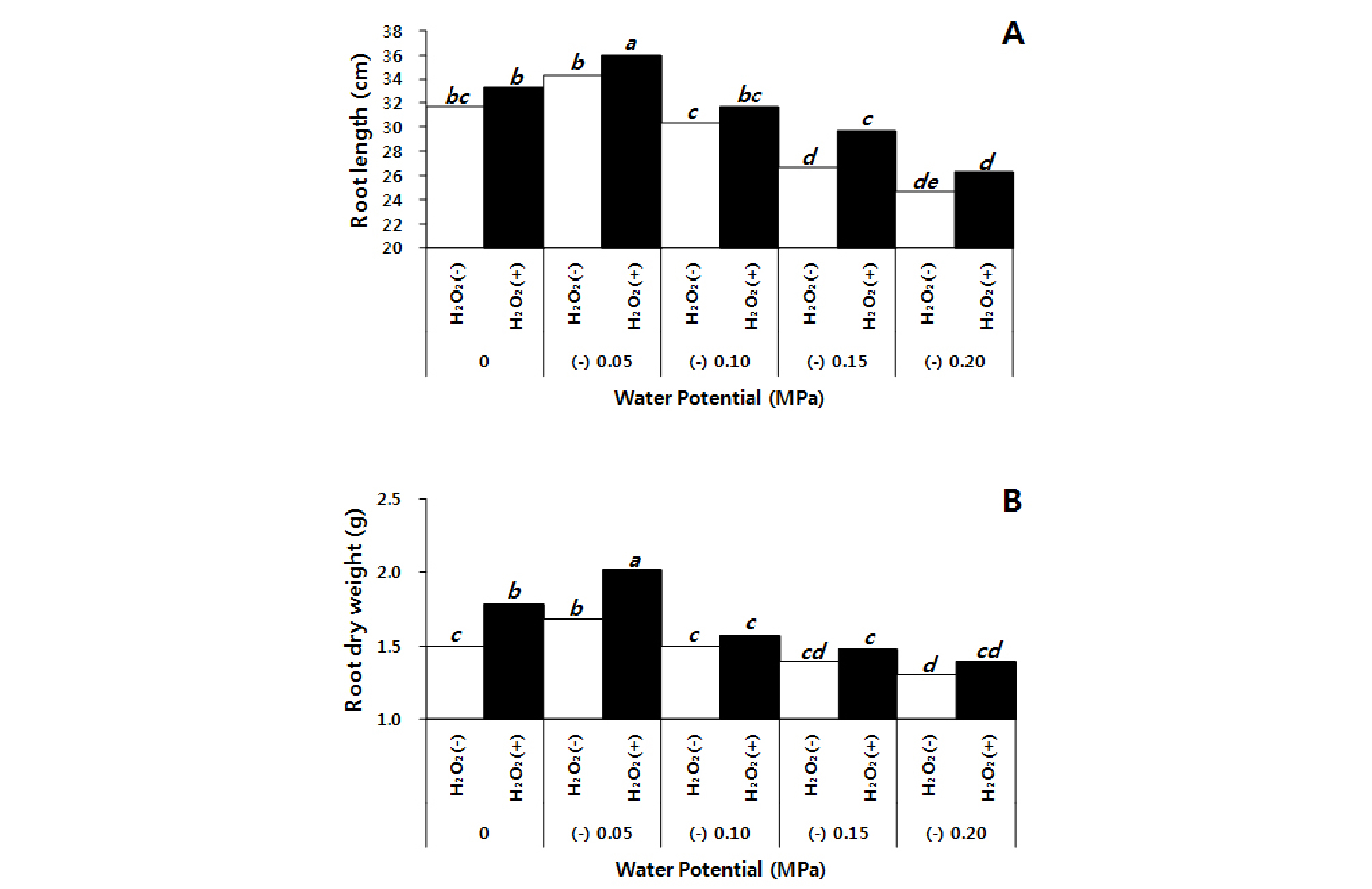
토양 수분퍼텐셜 0 ~ -0.20 MPa 조건에서 5주간 수수를 생육 시킨 결과, 초장은 전체적으로 토양 수분퍼텐셜이 낮아질수록 감소하는 경향을 보였으며, 포화상태(0 MPa)보다 포장용수량에 가까운 -0.05 MPa에서 가장 높은 생육정도를 보였다(Fig. 5A). 한편 수수에 10 mM 과산화수소 처리가 무처리 보다 초장이 전체적으로 0.8 ~ 3.0 cm 증가하였다(Fig. 5A). 줄기 직경은 과산화수소 처리가 무처리 보다 0.07 ~ 0.51 mm 증가하였으며(Fig. 5B), 지상부의 건물중은 과산화수소 처리에서 무처리 보다 5.1% ~ 16.8% 높은 건물량을 보였다(Fig. 5C). 이는 초장과 줄기 직경이 두꺼웠던 것에 비례하여 증가한 것으로 보인다.
과산화수소 처리가 수분 스트레스 하에서 수수의 발근의 미치는 영향을 보면, 모든 수분퍼텐셜에서 무처리 보다 과산화수소 처리에서 4.4 ~ 11.2% 뿌리 길이가 길었고, -0.15 MPa에서 뿌리 길이 차이가 가장 크게 나타났다(Fig. 6A). 뿌리의 건물중은 과산화수소 처리가 무처리 보다 5.0% ~ 20.0% 증가된 건물량을 보였다(Fig. 6B). 이는 과산화수소 처리가 수수의 뿌리 신장에 긍정적인 영향을 주어 발근력을 높여 토양으로부터 수분 흡수를 원활하게 하여 지하부 뿐만아니라 지상부의 생육에 도움을 준 것으로 보인다.
광합성과 관련이 있는 엽록소함량은 모든 토양 수분퍼텐셜에서 과산화수소 처리가 무처리 보다 높은 SPAD 값을 보였는데, 0 MPa 조건에서 과산화수소 처리에 의해 엽록소함량이 3.1% 증가하여 가장 낮은 효과를 보였고, -0.20 MPa 조건에서 13.3% 차이를 보여 수분 스트레스가 심할 경우 그 효과가 크게 나타났다. 나머지 -0.05 ~ -0.15 MPa 조건에서도 10.1 ~ 11.4% 차이로 과산화수소 처리에서 엽록소함량이 증가하는 것으로 보였다(Fig. 7A). 엽록소형광 역시 무처리 보다 과산화수소 처리에서 높게 측정되었다. 그 차이는 0 MPa에서 가장 낮은 1.3% 증가하였고, -0.05 MPa에서 가장 큰 6.4% 증가를 보였으며, -0.10 ~ -0.20 MPa 조건에서는 1.8 ~ 2.6% 증가하는 결과를 보였다(Fig. 7B). 기공전도도 값은 과산화수소 처리에서 무처리 보다 16.6 ~ 61.0 mmol-2·s-1 높은 값을 보였다(Fig. 7C). 일반적으로 수분 스트레스하에서 작물은 기공을 폐쇄와 이에 따른 광합성 저하로 인하여 초장, 줄기 직경, 잎 등의 생육이 감소하게 된다(Chaves et al., 2009). 하지만 Yordanov et al. (2000)은 과산화수소를 처리하게 되면 기공이 개방되어 광합성에 필요한 이산화탄소 유입을 원활하게 하고, 잎의 말림을 최소화하여 빛을 받는 면적을 넓게 하는데 기여하여 광합성 효율을 높이는 효과가 있다고 보고하였으며 본 연구에서도 과산화수소 처리가 광합성 효율을 높이는 결과를 보였다(Fig. 7).
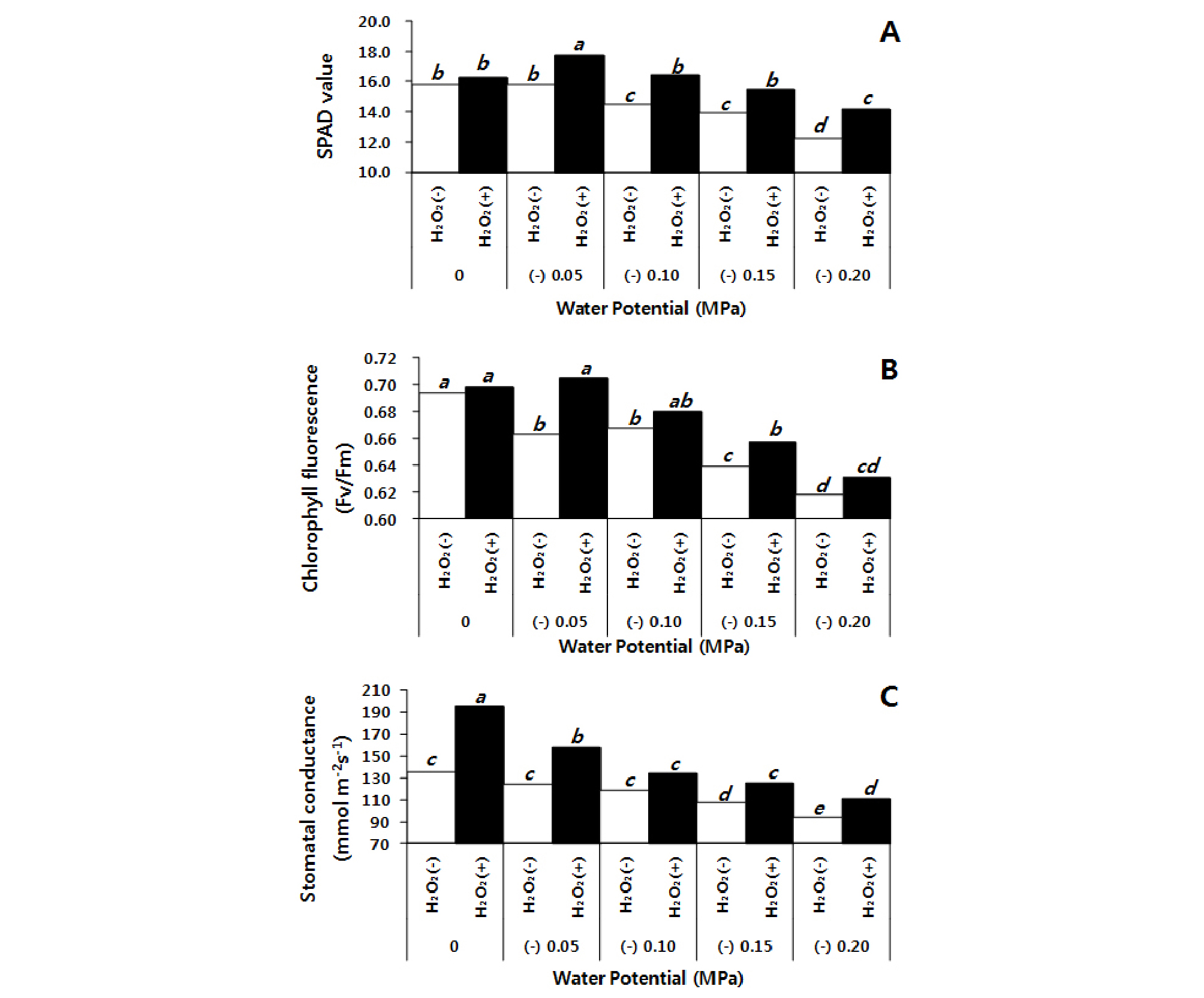
Fig. 7.
Influences of soil water potential and foliar application of H2O2 on SPAD value (A), chlorophyll fluorescence (B), and leaf stomatal conductance (C) of sorghum plants at 2 weeks after drought treatment. The different letters show significant difference (P < 0.05) as determined by Duncan’s multiple range test.
수수 식물체내 수분퍼텐셜은 토양 수분퍼텐셜이 -0.05 MPa에서 가장 낮은 2.7%, -0.15 MPa에서 가장 높은 4.5% 차이가 났다. 이 외의 토양 수분퍼텐셜 조건에서는 과산화수소 처리에서 무처리 보다 4.0 ~ 4.4% 높은 수분포텐셜을 보였다. 일반적으로 물의 순환에서 식물 잎의 수분포텐셜이 대기와 동일 -20 ~ -30 MPa 상태가 되면 영구위조점에 도달하는데 무처리의 경우 토양수분함량이 -0.15 ~ -0.2 MPa에서 체내 수분포텐셜이 -20 MPa 이상으로 영구위조점에 도달한 것으로 보인다. 반면, 과산화수소 처리는 -10 ~ -15 MPa 사이의 체내 수분포텐셜을 보였다(Fig. 8A). 수분 스트레스를 받게 되면 근계가 발달되지 못해 양분과 수분의 흡수가 저하되고(Egamberdieva et al., 2006), 뿌리로부터 수분이 흡수가 되지 않아 잎의 수분퍼텐셜과 상대함수량이 감소하고 이에 따라 광합성이 저하되고 건물중이 감소하게 된다(Park, 1995, Choi et al., 1997). 하지만 과산화수소 처리는 근계 발달을 도와 한발 스트레스 하에서도 수분을 원활하게 흡수, 유지함으로서 상대적으로 수수의 수분퍼텐셜이 증가한 것으로 보여진다(Faize et al., 2011). 지상부의 수분 함량은 초장, 줄기 직경이 두껍고 광합성능력이 높았던 과산화수소 처리가 무처리 보다 1.8% ~ 36.2% 더 많은 수분 함량을 보였으며, 수분 스트레스가 증가할수록 수분 함량의 차이도 크게 나타났다(Fig. 8B). 지하부의 수분 함량은 과산화수소 처리가 무처리 보다 6.4 ~ 18.0% 많은 수분을 함유하고 있었고 토양 수분퍼텐셜이 -0.05 MPa에서 가장 큰 차이를 보였다(Fig. 8C).
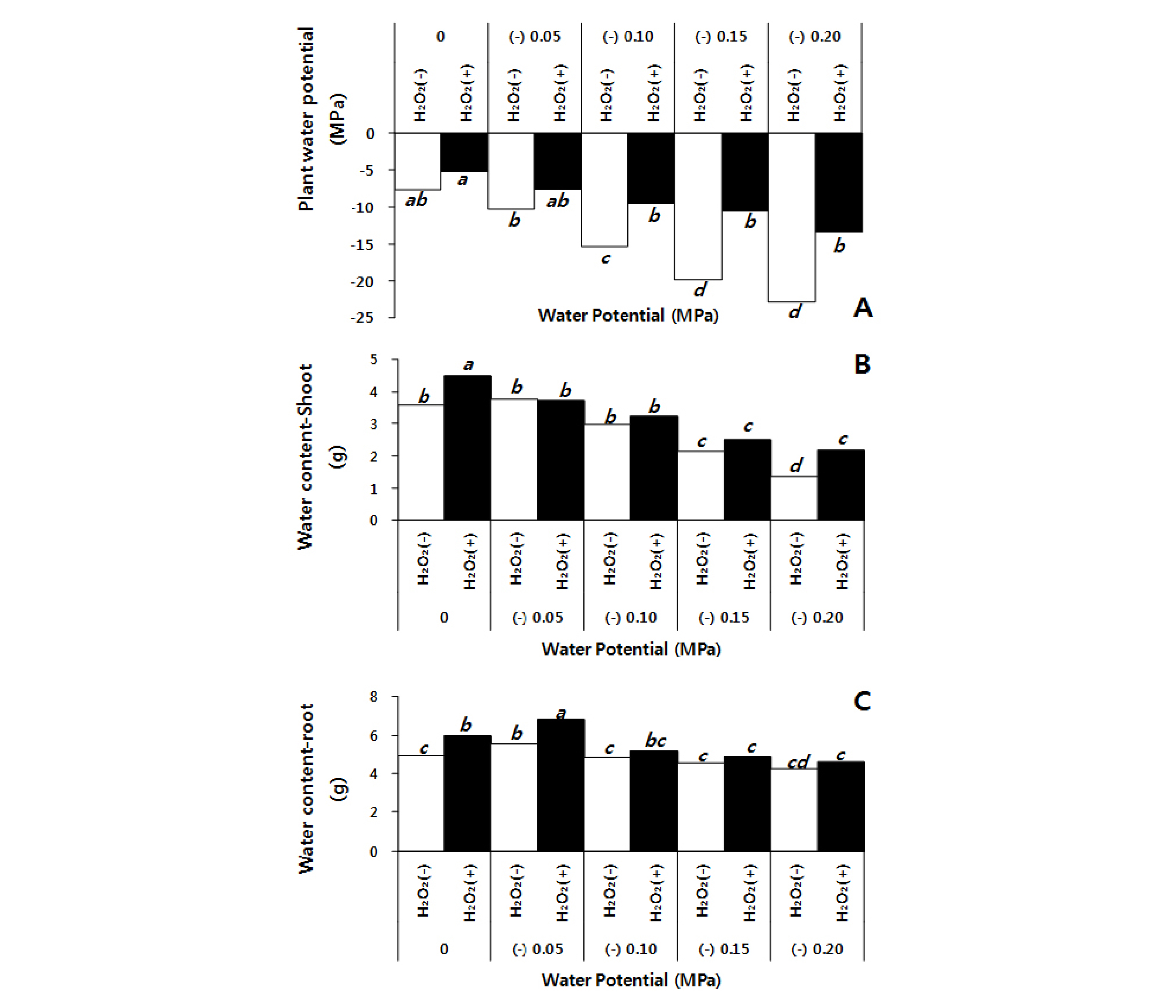
Fig. 8.
Influences of soil water potential and foliar applied H2O2 on plant water potential (A), shoot water content (B), and root water content (C) of sorghum plants at 5 weeks after drought treatment. The different letters show significant difference (P < 0.05) as determined by Duncan’s multiple range test.
온실 실험을 통해 과산화수소 처리가 한발 및 수분 스트레스 하에서 수수의 생장 및 광합성능력에 긍정적인 영향을 주는 것으로 조사되었다. 과산화수소 엽면처리를 하게 되면 한발 조건이 매우 심하더라도 항상 일정 수준의 기공 개도를 유지 할 수 있어 한발 조건에서도 이산화탄소 흡수가 가능하여 정상적인 광합성이 이루어질 수 있게 된다(Brestic et al., 1995). 옥수수에서 10 mM 과산화수소 처리는 삼투압에 영향을 주어 한발 스트레스 하에서 수분 흡수를 원활하게 하여 무처리 보다 식물체의 수분 함량과 잎의 수분퍼텐셜을 높여주고 이를 통해 잎 말림 현상도 감소하게 되어 광합성능력도 높여준다는 보고에서처럼 과산화수소는 엽내 수분 상태를 개선하여 본 연구 결과에서와 같은 광합성의 개선이 일어난 것으로 생각된다(Saglam et al., 2014).
적요
본 논문은 수수에 엽면처리된 과산화수소의 한발 스트레스 완화 효과가 있는지 알아보기 생리적 연구를 실시하였다.
수분 스트레스가 가장 심한 -0.15 MPa와 -0.20 MPa에서 과산화수소 처리에 의한 발아율 증가가 20%로 발아율의 차이가 가장 크게 조사되었다. 이는 과산화수소가 발아 과정에서 자극을 주어 대사 활성을 유도하여 수분스트레스가 심한 조건에서 일어나는 대사 저하가 완화되었기 때문으로 보인다.
1.수분 스트레스 하에서 10 mM 과산화수소 처리는 무처리 보다 20% 높은 발아율을 보였고, 유아·유근의 신장을 촉진하였다.
2.온실 pot 실험 결과 한발 하에서 과산화수소 처리는 형태적 형질(초장, 줄기 직경, 엽장, 엽수)과 생리적 형질(SPAD, 엽록소형광, 기공전도도) 모두 증가시켰다. 토양수분 구배장치를 이용한 실험 결과 역시 과산화수소 엽면처리가 광합성능력(SPAD, 기공전도도)과 뿌리 발근(지하부 건물중, 뿌리길이)이 우수하여 생육, 건물 생산량이 무처리 보다 높았다.
결과적으로 과산화수소의 처리는 수수의 발아율 향상과 기공 폐쇄를 억제하여 광합성능력을 향상시켰다. 이를 통해 한발 스트레스 대한 내성을 높여 수수의 생육을 유지 및 회복시켜 주었다.